FDA批准SuVax™用于预防和暴露后预防苏丹埃博拉病毒感染的孤儿药资格
在当前全球疫情不断肆虐的背景下,针对致命疾病的疫苗研发显得尤为紧迫而重要。近日,美国食品和药物管理局(FDA)的一项重要决定再次将人们的目光聚焦在疫苗领域。Soligenix, Inc.(以下简称Soligenix)宣布,其新型疫苗SuVax™已获得FDA的孤儿药资格,这标志着在预防和暴露后预防苏丹埃博拉病毒感染方面迈出了重要一步。
目录
SuVax™药物资格获批
2024年4月11日,Soligenix公司宣布其针对苏丹埃博拉病毒(SUDV)的疫苗SuVax™已被FDA孤儿产品开发办公室授予孤儿药称号。这一称号意味着SuVax™的活性成分,即重组表达的SUDV亚单位蛋白疫苗糖蛋白,被认可用于预防SUDV感染,无论是预防性接种还是暴露后的预防。
孤儿药法案的重要性
美国孤儿药法案的实施旨在支持和鼓励针对罕见疾病和病症的药物开发。这些罕见疾病往往影响人数较少,但对患者和其家庭来说却具有极大的负担。Soligenix的SuVax™之所以获得孤儿药资格,不仅在于其针对罕见疾病的目标,更因其具备的潜在市场优势。孤儿药指定将为Soligenix提供七年的市场独家销售权,使其能够充分利用财务和监管上的利益,加速临床试验进程并减轻开发成本。
SuVax™的独特之处
SuVax™是一种基于新型疫苗平台的疫苗,该平台整合了多项关键技术,包括稳健的蛋白质制造工艺、新型纳米乳剂佐剂以及热稳定的配制程序。Soligenix公司的高级副总裁兼首席科学官Oreola Donini博士表示,这种疫苗的独特之处在于将佐剂和抗原合二为一,为对抗SUDV等致命病毒提供了有力保障。实验结果表明,SuVax™疫苗在非人类灵长类动物中实现了100%的保护率,为其在临床应用中奠定了坚实基础。
SuVax™的技术特点
SuVax™是一种重组表达的SUDV糖蛋白亚单位蛋白疫苗,由Soligenix与夏威夷大学马诺阿分校的Axel Lehrer博士共同合作开发。该疫苗含有SUDV表面的蛋白质,能够在不引发感染风险的情况下诱导免疫反应。此外,SuVax™还采用一种新型佐剂,能够刺激体液和细胞介导的免疫反应,提高疫苗的免疫原性。这种佐剂已被公认为安全的赋形剂(GRAS),并且使得疫苗可以通过冷冻干燥技术制备成热稳定的粉末形式,大大方便了运输和储存。
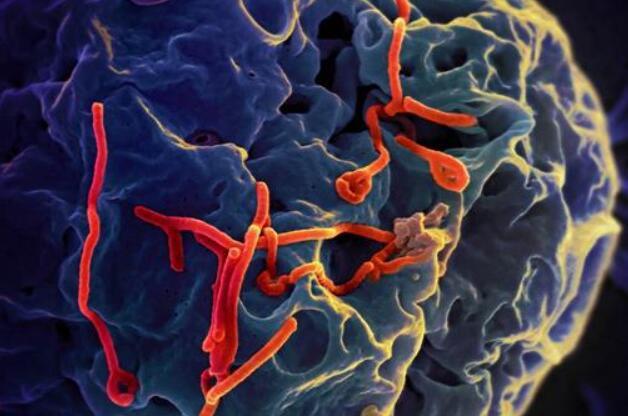
关于苏丹埃博拉病毒感染
埃博拉样疾病是由六种埃博拉病毒中的一种引起的,其中包括SUDV,是导致人类感染的第二大常见原因。埃博拉病毒属于丝状病毒科,与同科的马尔堡病毒等同样具有高度致命性的病毒共享相似的传播方式。
随着全球范围内埃博拉病毒等致命疾病的不断威胁,Soligenix公司的SuVax™疫苗的获批意味着在抗击这些疾病的道路上又迈出了重要一步。其独特的技术优势和孤儿药资格的认定将为该疫苗的推广和应用提供强有力的支持,为保护人类健康作出了突出贡献。期待着SuVax™在未来的临床应用中展现出更加卓越的效果,为人类健康的未来带来希望和光明。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请谘询主治医师。