APHEXDA MOTIXAFORTIDE
【商品名称】:APHEXDA
【通用名称】:MOTIXAFORTIDE
APHEXDA-MOTIXAFORTIDE说明书
【Aphexda(motixafortide)生产厂家】
BioLineRx生物制药公司
【Aphexda(motixafortide)适应症】
Aphexda适用于与filgrastim (G-CSF)联合使用,以动员造血干细胞进入外周血,用于多发性骨髓瘤患者的采集和随后的自体移植。
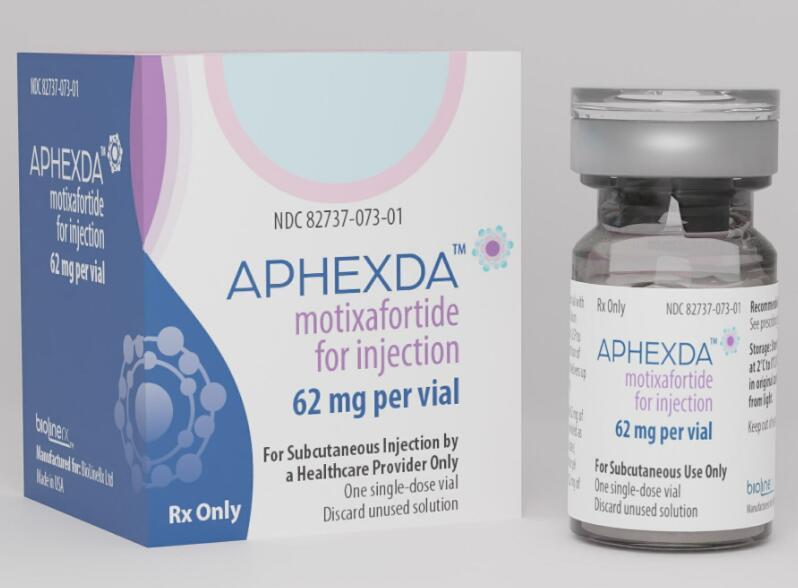
以上图片来源于网络
【Aphexda(motixafortide)规格】
62毫克/瓶
【Aphexda(motixafortide)用法用量】
1.在filgrastim被注射后开始Aphexda治疗,每天给药,持续4天。
2.推荐剂量为按实际体重1.25mg/kg,开始前10至14小时进行皮下注射。
3.第二剂Aphexda可在10至14小时后给药,在第三次单采之前。
请参阅完整的处方信息,了解有关准备的说明和管理。
【Aphexda(motixafortide)禁忌症】
Aphexda禁用于对motixafortide有严重过敏反应史的患者。
【Aphexda(motixafortide)作用机制】
motixafortide是C-X-C基序趋化因子受体4(CXCR4)的抑制剂,阻断其同源配体基质衍生因子-1α(SDF-1α)/C-X-C基序趋化因子配体12(CXCL12)的结合。SDF-1α和CXCR4在人类造血干细胞向骨髓室的运输和归巢中发挥作用。一旦进入骨髓,干细胞CXCR4可以直接通过SDF-1α或通过诱导其他粘附分子将这些细胞锚定在骨髓基质上。在小鼠、大鼠、狗和人类中,用莫替福肽治疗会导致白细胞增多,并使骨髓干细胞和祖细胞进入外周循环。在啮齿类动物移植模型中,通过莫替福肽动员的干细胞能够以长期的重新繁殖能力进行移植。
【Aphexda(motixafortide)贮藏】
在原始纸箱中以2°C至8°C(36°F至46°F)的温度储存,以避光。
•在冷藏2°C至8°C(36°F至46°F)或室温20°C至25°C(68°F至77°F)下避光保存24小时后,丢弃制备的复原溶液。
【Aphexda(motixafortide)注意事项】
①过敏性休克和过敏反应
出现过敏性休克和过敏反应。术前用药在每次使用Aphexda前约30-60分钟,所有患者均采用三联用药方案,包括H1抗组胺药、H2阻滞剂和白三烯抑制剂。在人员和治疗可立即用于治疗过敏反应和其他全身反应的环境中使用Aphexda。Aphexda给药后监测患者1小时,并及时处理反应。接受负性变时性药物(如β-受体阻滞剂)的患者在出现过敏反应时可能更容易发生低血压,在适当的情况下,这些药物应替换为非变时性药物。
②注射部位反应
出现了注射部位反应(73%),包括疼痛(53%)、红斑(27%)和瘙痒(24%)。9%的患者出现严重反应。每次使用Aphexda前,先服用镇痛药物(如对乙酰氨基酚)。根据需要,在给药后使用止痛药物和局部治疗。
③白血病患者的肿瘤细胞动员
为了动员造血干细胞(HSC), Aphexda可能会动员白血病细胞并随后污染单采产品。因此,Aphexda不适用于白血病患者的HSC动员和采集。
④白细胞增多
Aphexda与filgrastim联合用药可增加循环白细胞和HSC数量。Aphexda使用期间监测白细胞计数。
⑤肿瘤细胞动员的潜力
当Aphexda与filgrastim联合用于HSC动员时,肿瘤细胞可能从骨髓中释放出来,随后被收集在白细胞分离产物中。肿瘤细胞潜在回输的效果还没有得到很好的研究。
⑥胚胎-胎儿毒性
基于其作用机制,Aphexda可导致胎儿损伤。告知孕妇对胎儿的潜在风险。在开始使用Aphexda进行治疗之前,验证具有生殖潜力的女性的妊娠状态,并建议在治疗期间和最后一次给药后8天内使用有效的避孕措施。
【Aphexda(motixafortide)不良反应】
接受Aphexda治疗的患者最常见的不良反应(发生率> 20%)为注射部位反应[73%,包括疼痛(53%)、红斑(27%)、瘙痒(24%)];瘙痒(38%);潮红(33%);背痛(21%)。
以上资料只供参考,详情请咨询医生建议。更多药品信息可与我们的药剂师客服联系查询!
【温馨提示】
如需要更多Aphexda(motixafortide)资讯,欢迎与致泰药业联络查询。香港致泰药业是经香港政府卫生署注册的药品批发商,专注于全球新特药品进出口业务。