15
9月
改善A型血友病治疗:FDA接受Altuviiio更新标签
A型血友病,又称甲型血友病,是一种罕见的遗传性疾病,特点是凝血蛋白VIII水平降低,导致患者容易发生出血。这种疾病对患者的生活质量产生了极大的影响,尤其是对于年幼的患者。近期,美国食品药品监督管理局(FDA)接受了Altuviiio的补充生物制品许可申请,将该药物的使用扩展到12岁以下患有严重A型血友病的儿童患者。这一决定基于关键的临床研究数据,为改善患者的治疗提供了新的希望。 Altuviiio的背景 Altuviiio,通用名为抗血友病因子(重组),FC-VWF-XTEN融合蛋白,是一种高持续性因子VIII替代疗法。它旨在提供有效的出血保护,降低A型血友病患者的出血风险。此前,FDA已经批... 查看详情
14
9月
FDA授予Tulmimitostat治疗子宫内膜癌症的快速通道地位
子宫内膜癌(endometrial cancer)是一种妇女常见的癌症,但对于某些患者,特别是那些病情晚期、复发或转移的患者,治疗一直是一个巨大的挑战。近期,美国食品药品监督管理局(FDA)为一种新型药物Tulmimetostat(CPI-0209)授予了“快速通道”地位,为这些患者提供了新的治疗选择。 Tulmimetostat:新希望 Tulmimetostat,又称CPI-0209,是一种第二代EZH2/EZH1抑制剂,旨在通过延长与靶点的结合时间,实现全面的靶点覆盖。这一药物的研发是为了治疗一种特定亚型的子宫内膜癌,即携带ARID1A突变的癌症。ARID1A突变使得肿瘤更难治疗,因为它... 查看详情
13
9月
BRL03针对肺癌、胃癌及其他先进实体瘤临床试验获FDA批准
癌症是一项全球性的健康挑战,而肺癌、胃癌以及其他先进期实体瘤则是其中的重要组成部分。然而,在新加坡,生物科技公司Biosyngen Pte Ltd于2023年9月9日宣布,美国FDA已批准其针对肺癌、胃癌和其他先进期实体瘤治疗的BRL03一期/二期临床试验的探索性新药(IND)申请。这一批准标志着Biosyngen在细胞免疫治疗领域取得的又一重大突破。 值得注意的是,BRL03还是Biosyngen首次进入临床试验的TCR-T疗法。这一重大成就要归功于公司多年来的尖端技术和广泛积累的能力与资源。 IDENTIFIER技术平台的背后支持 Biosyngen的IDENTIFIER技术平台为抗原、抗... 查看详情
13
9月
PMB-CT01 B细胞非霍奇金淋巴瘤一期临床试验首剂组成功,二期组即将开启
2023年9月11日,加利福尼亚尔维恩(IRVINE, Calif.)— 临床阶段生物科技公司PeproMene Bio, Inc. 宣布,其针对复发性或难治性B细胞非霍奇金淋巴瘤(r/r B-NHL)的一期临床试验PMB-CT01(BAFFR-CAR T细胞)的首个剂量队列已经完成。在此队列中,未观察到剂量限制性毒性(DLT),因此该研究已获批准继续进行下一个队列的试验。本次PMB-102试验在国内最大的癌症研究与治疗机构之一——“希望之城”(City of Hope)进行。PeproMene公司从“希望之城”获得了PMB-CT01相关的知识产权。 首剂队列结果 在首个队列中,给予50... 查看详情
13
9月
TAK-279治疗活动性牛皮癣性关节炎的2b期研究获得积极顶线结果
2023年9月11日,日本大阪和美国剑桥,武田制药(Takeda)宣布了一项重要的临床试验顶线结果,该试验评估了一种名为TAK-279的高度选择性口服酪氨酸激酶2(TYK2)抑制剂的疗效,用于治疗活跃性牛皮癣性关节炎(psoriatic arthritis)。这项研究取得了积极的结果,显示与安慰剂相比,TAK-279每日一次治疗的患者在12周时达到了至少20%改善疾病体征和症状的ACR20反应的比例明显更高,支持其作为治疗牛皮癣性关节炎患者的高度选择性口服药物的潜力。此次试验的安全性和耐受性与以前的TAK-279临床试验一致。结果分析仍在进行中,武田制药计划在即将举行的医学会议上呈现临床结果。... 查看详情
13
9月
探索性分析显示:Sotatercept有望改善肺动脉高压患者的生存前景
2023年9月11日,美国默克(NYSE:MRK)在欧洲呼吸学会(European Respiratory Society,ERS)国际大会2023上发布了关于其肺动脉高压(PAH)新型调节素信号抑制剂生物制剂Sotatercept的研究新分析。一项对来自第3期STELLAR研究的患者进行的右心导管检查和超声心动图数据的探索性事后分析显示,与背景治疗相结合使用Sotatercept治疗24周可以减小右心的大小,改善右心室(RV)功能和血流动力学状况。这一分析在口头报告中亮相,并同时发表在《European Respiratory Journal》上。此外,还介绍了第3期SOTERIA开放性延长... 查看详情
12
9月
新数据显示Qelbree改善注意缺陷与多动障碍(多动症)症状
注意缺陷与多动障碍(ADHD)是一种神经行为障碍,通常在儿童时期发现,但也可能持续到成年。这种疾病会影响一个人的注意力、活动水平和自我控制能力。 2023年9月9日,马里兰州罗克维尔。生物制药公司Supernus Pharmaceuticals, Inc.专注于研发和商业化中枢神经系统疾病治疗产品,宣布在2023年Psych Congress上展示了两份海报,展示了将Qelbree添加到兴奋剂治疗中的6岁及以上ADHD患儿以及长期服用Qelbree的成年ADHD患者疗效提高的新数据。 首席医疗官兼研发高级副总裁Jonathan Rubin表示:“尽管ADHD被认为是最常见的精神疾病之一,影响了... 查看详情
12
9月
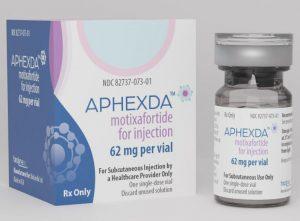
FDA批准Aphexda(motixafortide)动员造血干细胞用于多发性骨髓瘤患者的自体移植
2023年9月11日,以色列的BioLineRx Ltd.(纳斯达克/TASE: BLRX)宣布,美国食品药品监督管理局(FDA)已批准Aphexda™(motixafortide)与filgrastim(G-CSF)联合使用,以促使多发性骨髓瘤患者的造血干细胞进入外周血,供采集并进行自体移植治疗。Aphexda通过注射皮下给药。 多发性骨髓瘤是第二常见的血液恶性肿瘤。自体干细胞移植(ASCT)是多发性骨髓瘤标准治疗范式的一部分,为这种癌症患者提供了延长生存的机会。ASCT的成功取决于治疗过程中足够的干细胞移动。美国移植和细胞治疗学协会(ASTCT)的指南建议收集3-5 x 10 CD34+细... 查看详情
12
9月
WHIM综合征的突破!口服CXCR4拮抗剂Mavorixafor向FDA提交新药申请
WHIM综合征,一种罕见的常染色体显性联合免疫缺陷病,一直以来没有明确的治疗方法,给患者的生活带来了巨大困扰。这种疾病的复杂多变表现与CXCR4/CXCL12信号通路的异常有关,导致免疫系统失调,使患者容易感染、发展疣和其他并发症。然而,近期,一项令人振奋的消息出现了:X4制药公司已向美国食品药品监督管理局(FDA)提交了一份新药申请,旨在批准Mavorixafor用于WHIM综合征的治疗。这一口服药物有望成为首个专门针对这种疾病的治疗方法。 WHIM综合征:复杂多变的疾病 WHIM综合征是一种少见的遗传性疾病,其名称代表了其主要临床表现:疣、低丙种球蛋白血症、感染和骨髓增生异常。这种综合征的... 查看详情
12
9月
阿尔茨海默氏症Senolytics疗法清除大脑中淀粉样蛋白,降低血液中的炎症
阿尔茨海默氏症,一种神经退行性疾病,如今已经成为老年人群中的一大威胁。随着世界范围内人类寿命的不断延长,老年化社会逐渐加剧,阿尔茨海默氏症患者数量也呈持续上升的趋势。据估计,到2050年,全球阿尔茨海默氏症患者将达到1.5亿以上。这一数字引起了广泛的担忧,促使科学家不断探索治疗此病的新途径。近期的研究为我们带来了新的曙光,一种被称为“Senolytics疗法”的联合治疗方式,有望为阿尔茨海默病患者带来希望。 阿尔茨海默氏症:老年人群的威胁 阿尔茨海默氏症是一种隐匿而进行性发展的神经退行性疾病,患者通常会经历认知功能逐渐下降、失忆、情感波动等症状,最终导致严重的认知障碍和日常生活能力的丧失。据统... 查看详情