07
11月
FDA批准Zituvimet(西他列汀和盐酸二甲双胍)治疗成人2型糖尿病患者
2023年11月6日,印度艾哈迈达巴德—Zydus生命科学有限公司(以下简称“Zydus”)宣布,美国食品和药物管理局(FDA)已批准其新药申请(NDA)的“Zituvimet”(西他列汀和盐酸二甲双胍)片剂,包括50毫克/500毫克和50毫克/1000毫克两种规格。 Zituvimet包含活性成分西他列汀,一种二肽肽酶-4(DPP-4)抑制剂,以及盐酸二甲双胍(HCl),一种双胍类药物,用于辅助饮食和锻炼,改善2型糖尿病成年患者的血糖控制。 Zituvimet的批准基于Zydus团队进行的研究、开发、监管和生产工作。Zituvimet已根据当前USFDA标准进行亚硝胺和潜在的基因毒性杂质的质... 查看详情
07
11月
FDA审查N-803(Anktiva)联合卡介苗疫苗:非肌层浸润性膀胱癌新曙光
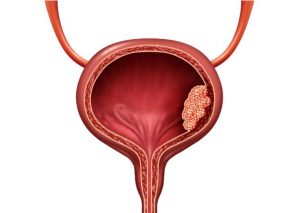
膀胱癌,一种恶性肿瘤,常发生在膀胱黏膜上,是泌尿系统中最普遍的癌症之一。非肌层浸润性膀胱癌(NMIBC)占膀胱癌的绝大多数,而卡介苗是目前治疗该疾病的标准疗法。然而,对于一部分患者而言,卡介苗可能无效。最近,ImmunityBio公司推出了一项潜在的突破性治疗,N-803(商品名Anktiva)联合卡介苗疫苗,正受到美国食品药品监督管理局(FDA)的审查,为NMIBC患者带来新的希望。 N-803:重塑免疫系统的利器 N-803是一种抗体细胞因子融合蛋白,其核心作用是增强免疫系统的功能。它通过超拮抗细胞因子白细胞介素-15(IL-15)的作用,刺激自然杀伤细胞和T细胞的增殖,从而增强了免疫反应... 查看详情
06
11月
FDA授予Obisbemeda(186Re)治疗乳腺癌和蛛网膜脑膜转移孤儿药资格
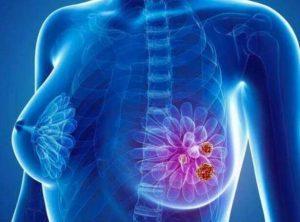
乳腺癌和蛛网膜脑膜转移是妇女健康领域的严重挑战,迫切需要新的治疗方法。近期,FDA授予Obisbemeda(186Re)孤儿药资格,这一新型放射治疗药物展现出潜力,有望填补乳腺癌和蛛网膜脑膜转移患者的治疗空白。 Obisbemeda(186Re):放射治疗的创新突破 Obisbemeda(186Re)是一种新型的可注射放射治疗药物,能够高度精准地照射中枢神经系统转移瘤,对病变组织施加高剂量的辐射。该药物目前正在进行ReSPECT-LM试验(NCT05034497)的第1/2a阶段,用于治疗蛛网膜脑膜转移患者,同时也在ReSPECT-GBM试验(NCT01906385)的第1/2阶段中用于治疗复... 查看详情
06
11月
欧盟批准RYEQO(Relugolix复方片)用于子宫内膜异位症对症治疗的商业化
2023年11月2日,匈牙利的Gedeon Richter Plc.(简称Richter)、以及Sumitomo Pharma America, Inc.(简称SMPA)和Sumitomo Pharma Switzerland, GmbH(简称SMPS)联合宣布,欧洲委员会(简称EC)已批准RYEQO®(relugolix 40毫克,雌二醇1.0毫克和醇诺酮醋酸酯0.5毫克)用于症状性治疗曾接受先前医疗或外科治疗的子宫内膜异位症女性。这一决定是在欧洲药品管理局(EMA)人类用药品委员会(CHMP)于2023年9月15日发表积极意见后作出的,并适用于欧洲联盟的所有成员国。 RYEQO®最初于20... 查看详情
06
11月
II期ALTITUDE试验揭示ABBV-RGX-314治疗糖尿病性视网膜病变的一年积极数据
2023年11月4日,REGENXBIO公司宣布他们在进行中的ABBV-RGX-314治疗糖尿病性视网膜病变(DR)的II期ALTITUDE试验获得了额外的积极数据。这项试验使用办公室超脉络膜输送方式进行,针对不涉及中央糖尿病黄斑水肿(CI-DME)的患者。数据将由亚利桑那州视网膜顾问Mark Barakat博士在美国旧金山举行的美国眼科学会会议上进行发布。ABBV-RGX-314正在研究作为潜在的一次性基因疗法,用于湿性年龄相关性黄斑变性、DR和其他慢性视网膜疾病的治疗。 “我们很高兴看到ABBV-RGX-314在剂量2下继续良好耐受,并为非增生性DR患者呈现出具有临床意义的改善... 查看详情
06
11月
FDA批准混合现实手术指导STELLAR KNEE用于全膝关节置换术手术
2023年11月03日,混合现实技术取得了重大突破,POLARIS AR宣布他们的STELLAR KNEE获得了美国食品和药物管理局(FDA)的510(k)批准。这一批准将开启一项全新的数字手术室革命,为外科医生提供了前所未有的实时解剖数据访问能力,用于全膝关节置换手术的测量、规划和指导。本文将深入探讨STELLAR KNEE的背后技术、其潜在应用以及对医疗领域的影响。 混合现实技术:手术引导的未来 STELLAR KNEE的背后是混合现实技术,这是一种将物理和虚拟世界相结合的先进技术。POLARIS AR致力于创造混合现实手术指导的全新领域,使外科手术变得更为精准和可控。通过混合现实显示器,... 查看详情
06
11月
KRAZATI(Adagrasib)治疗KRAS-G12C突变非小细胞肺癌在英国获批
2023年11月03日,医学界传来了一条令人振奋的消息:英国药品和保健品监管局(MHRA)正式批准了KRAZATI®(也称adagrasib)的条件营销授权,作为一项独特的疗法,用于治疗晚期非小细胞肺癌(NSCLC)患者中的KRAS G12C突变。这个突破性的决定将改变数百万患者的生活,特别是那些先前接受铂类药物治疗后病情进展或对化疗和/或抗 PD-1/PD-L1 免疫疗法不耐受的患者。 突破性决定的背后 KRAZATI的获批是建立在KRYSTAL-1开放标签1/2期多次扩展队列试验的基础上。这项试验旨在评估adagrasib作为单一疗法以及与其他抗癌疗法联合治疗,用于治疗晚期实体瘤患者,特别... 查看详情
03
11月
Elranatamab有望获得欧盟对严重预治疗复发/难治性多发性骨髓瘤的批准
多发性骨髓瘤是一种复杂多变的血液肿瘤,对于曾接受多轮治疗的患者而言,找到有效的治疗方案变得尤为重要。近期,欧洲药物管理局(European Medicines Agency)人类用药品委员会(Committee for Medicinal Products for Human Use,CHMP)推荐批准Elranatamab-bccm(商品名:Elrexfio)用于成年患者的治疗,这些患者已经曾接受3种或更多疗法,包括免疫调节剂、蛋白酶体抑制剂和抗CD38单克隆抗体,且在上一疗法中疾病有进展。 新曙光:Elranatamab-bccm的药物认可 Elranatamab-bccm,商业名称Elr... 查看详情
03
11月
欧盟已接受康奈非尼/比美替尼治疗BRAF V600+晚期非小细胞肺癌的营销授权申请
非小细胞肺癌(NSCLC)一直是全球癌症患者的主要杀手之一。然而,针对不同亚型的NSCLC,针对性的治疗选择仍然有限。最近,一项提交给欧洲药品管理局(EMA)的营销授权申请(MAA)为一种新的治疗方法提供了新的希望。康奈非尼Braftovi(Encorafenib)和比美替尼Mektovi(Binimetinib)的组合治疗可能会成为BRAF V600突变型晚期NSCLC患者的新希望。 PHAROS试验数据支持申请 欧洲药品管理局已经接受了提交的MAA,申请批准康奈非尼(Encorafenib)和比美替尼(Binimetinib)的组合治疗,用于治疗未接受治疗或之前接受过治疗的BRAF V60... 查看详情
03
11月
非侵入性治疗帕金森病:FDA接受SPN-830阿扑吗啡输液装置新药申请审查
美国生物制药公司Supernus Pharmaceuticals, Inc.(Nasdaq: SUPN)日前宣布,美国食品和药物管理局(FDA)已批准其新药申请(NDA)重新提交,用于其阿扑吗啡注射装置(SPN-830),以持续治疗帕金森病(PD)患者的运动波动(OFF阶段),预计审批时间为2024年4月5日。这一决定标志着Supernus在中枢神经系统疾病治疗领域的巨大突破,为帕金森病患者带来了全新的、非侵入性的治疗选择。 创新治疗:SPN-830注射装置 帕金森病是一种中枢神经系统疾病,通常伴随着运动障碍、肌肉僵硬和震颤等症状。患者经常会在治疗过程中出现运动波动,即”OFF&#... 查看详情