19
12月
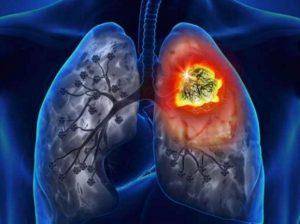
Tarlatamab治疗晚期小细胞肺癌获FDA优先审查
在肺癌治疗领域,尤其是晚期小细胞肺癌(SCLC)患者,寻找更有效的治疗方法一直是医学界的追求目标。近日,一项备受瞩目的药物——Tarlatamab,由安进公司研发,获得了美国食品药品监督管理局(FDA)的优先审查资格。本文将深入探讨Tarlatamab的研发背景、临床试验结果以及对晚期小细胞肺癌患者的潜在影响。 Tarlatamab的研发背景 Tarlatamab是一种新型的同类首创双特异性T细胞接合免疫疗法,其设计目标是靶向SCLC细胞上的δ样配体3和T细胞上的CD3。该药物被设计用于治疗那些在以铂类为基础的化疗后或期间,出现疾病进展的成年SCLC患者。 临床试验结果 支持Tarlatama... 查看详情
18
12月
FDA授予Naporafenib在晚期NRAS突变黑色素瘤中的快速通道认定
近期,Erasca公司宣布其首个全口服药物Naporafenib在治疗晚期NRAS突变黑色素瘤方面获得了美国食品和药物管理局(FDA)的快速通道认定。这一认定使得该药物在治疗患有此类疾病的患者中更快地获得可能,为填补当前存在的医学需求提供了可能的解决方案。 重要里程碑:NRAS突变黑色素瘤的治疗突破 Naporafenib是一种口服药物,属于pan-RAF抑制剂,具有在晚期NRAS突变黑色素瘤和其他RAS/MAPK途径改变的固体肿瘤中成为首个和最佳选择的潜力。截至目前,Naporafenib已在500多名患者中进行了用药试验,确立了其在多个适应症中的安全性、耐受性和初步概念验证。 突破性临床试... 查看详情
18
12月
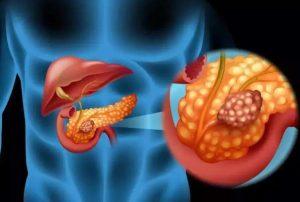
FDA授予CAN-2409在胰腺癌治疗中的快速通道认定
Candel生物制药公司宣布,美国食品和药物管理局(FDA)已授予其首席调查腺病毒资产CAN-2409加前体(瓦拉西克洛韦)快速通道认定,用于治疗胰腺导管腺癌(PDAC)以改善总体生存率。 快速通道认定的重要性 “我们对FDA决定在胰腺癌治疗中为CAN-2409授予快速通道认定感到高兴,” Candel总裁兼首席执行官Paul Peter Tak博士表示。 “这一里程碑来自我们在边缘可切除PDAC患者中进行的随机2期临床试验的首个中期数据报告,该报告显示在用CAN-2409实验性治疗后,患者的生存时间延长并保持稳定,特别是当与接受放疗治疗的患者的真实世界数据... 查看详情
18
12月
美国FDA授予Nana-val治疗鼻咽癌的孤儿药物认定
加利福尼亚州圣迭戈,2023年12月12日 — 珍视生物(Viracta Therapeutics,股票代码:VIRX),一家专注于治疗全球范围内影响患者的病毒相关癌症的临床阶段精准肿瘤学公司,今天宣布,美国食品和药物管理局(FDA)已授予孤儿药物认定(ODD)给Nana-val(Nanatinostat与Valganciclovir联合使用),该公司的口服调查性疗法,旨在治疗爱泼斯坦-巴尔病毒(EBV)相关的癌症,特别用于鼻咽癌(NPC)。这是Nana-val在EBV阳性(EBV)实体瘤以及EBV相关淋巴瘤以外首次获得的孤儿药物认定。此前,FDA已经为Nana-val在T细胞淋巴瘤、移植后淋... 查看详情
17
12月
FDA批准ZORYVE(Roflumilast)泡沫剂治疗9岁及以上脂溢性皮炎
2023年12月15日,Arcutis Biotherapeutics, Inc.在美国食品和药物管理局(FDA)的批准下,宣布了一项具有划时代意义的决定:ZORYVE®(Roflumilast)0.3% 泡沫剂正式获批,成为治疗9岁及以上脂溢性皮炎的创新药物。这一消息标志着全球范围内脂溢性皮炎患者迎来了更为便捷、高效的治疗选择。 1. 科学突破:Roflumilast泡沫剂的新作用机制 ZORYVE®的获批是一项医学上的突破,作为每日一次的无类固醇泡沫,它创新性地应用了磷酸二酯酶4(PDE4)抑制剂,为脂溢性皮炎的治疗注入了新的生机。这是20多年来首个获批用于脂溢性皮炎的药物,将为患者带来更... 查看详情
17
12月
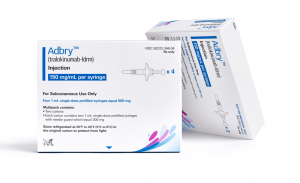
FDA批准Adbry(Tralokinumab)治疗12-17岁中度至重度特应性皮炎
2023年12月15日,LEO Pharma Inc.宣布美国食品和药物管理局(FDA)批准Adbry®(Tralokinumab-ldrm)用于治疗12-17岁中度至重度特应性皮炎(AD)的儿科患者。这一批准标志着针对儿童免疫炎症疾病的新治疗选择的到来,为改善患者生活质量提供了新的希望。 1. 数据背后的科学突破:Adbry®的独特机制 Adbry®是第一个获得FDA批准的、特异性结合并抑制白细胞介素(IL)-13细胞因子的生物制剂。IL-13细胞因子在AD症状的形成中扮演关键角色,Adbry®的批准为针对这一疾病的治疗开辟了新的道路。 2. 试验数据揭示:Adbry®显著改善儿科患者症状 ... 查看详情
17
12月
FDA批准K药联合Padcev一线治疗局部晚期或转移性尿路上皮癌
2023年12月15日,默克公司(MSD)宣布其抗PD-1疗法帕博利珠单抗KEYTRUDA(K药)与抗体药物Padcev(enfortumab vedotin)联合用于治疗晚期或转移性尿路上皮癌成年患者已获得美国食品和药物管理局(FDA)批准。此次批准的依据是KEYNOTE-A39试验(EV-302)的数据,这标志着尿路上皮癌治疗领域迎来了一项重大突破。 1. 试验数据揭示:KEYTRUDA联合Padcev显著改善患者生存率 在涉及886名局部晚期或转移性尿路上皮癌患者的3期试验中,KEYTRUDA联合Padcev的疗效表现令人瞩目。相较于铂类化疗,该联合治疗使患者的总生存期(OS)和无进展生... 查看详情
16
12月
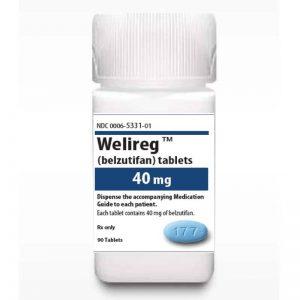
FDA批准Welireg(Belzutifan)用于经PD-1/PD-L1和VEGF-TKI治疗后晚期肾细胞癌
2023年12月14日,美国食品和药物管理局(FDA)宣布批准WELIREG(Belzutifan,贝组替凡),这是一种口服缺氧诱导因子2α(HIF-2α)抑制剂,专门用于治疗经过PD-1或PD-L1和VEGF-TKI治疗的晚期肾细胞癌(RCC)成年患者。这一决定为那些在先前治疗后病情进展的患者提供了新的治疗选择。 挑战:晚期RCC治疗的新里程碑 WELIREG的批准建立在LITESPARK-005试验的结果之上,该试验是唯一一个专门评估PD-1或PD-L1检查点治疗和VEGF-TKI治疗后病情进展的晚期RCC患者的研究。在试验中,WELIREG在接受PD-1或PD-L1检查点治疗后的晚期RC... 查看详情
15
12月
血友病A/B新型疗法Marstacimab正接受FDA和欧盟审查
在医学领域的不断创新中,辉瑞公司最新宣布的抗组织因子途径抑制剂Marstacimab的生物制剂许可申请(BLA)在治疗血友病A和B的新型疗法中引起广泛关注。该药物可能成为血友病患者的里程碑,为那些无法采取传统因子替代疗法的患者带来新的治疗选择。 血友病的背景 血友病是一种罕见的遗传性血液疾病,由于凝血因子的缺乏而引起,分为血友病A和B。传统治疗手段主要是采取凝血因子的替代,然而,对于一部分患者,尤其是产生了抑制剂的患者,传统疗法可能无效。这些抑制剂会妨碍正常的凝血因子作用,给患者带来更大的痛苦和风险。 Marstacimab的创新性 Marstacimab是一种抗组织因子途径抑制剂,采用每周一... 查看详情
15
12月
FDA批准Trogarzo(Ibalizumab)90秒静脉(IV)推入治疗多重耐药HIV感染者
2023年12月13日Theratechnologies Inc. 宣布HIV-1药物Trogarzo(ibalizumab-uiyk)的美国标签信息迎来一次重要更新,引入了90秒静脉推注剂量。这一创新治疗方案标志着HIV-1治疗领域的一项革命性进展,为患者提供更为便捷和灵活的用药选择。 HIV-1感染的背景 HIV-1感染是导致获得性免疫缺陷综合症(AIDS)的主要病原之一,具有较强的毒性和传染性。这一感染会损害免疫系统的白细胞,特别是CD4+细胞,导致患者出现一系列症状,如发热、皮疹、慢性疲劳等。Trogarzo作为一种重组人源化单克隆抗体,成为阻止HIV-1感染CD4+T细胞的重要工具。... 查看详情