21
3月
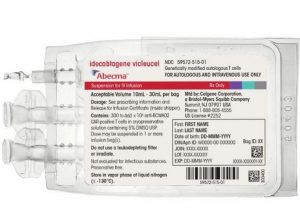
欧盟批准Abecma(ide-cel)用于治疗多发性骨髓瘤
2024年3月20日,百时美施贵宝公司宣布了一项重大突破:欧盟委员会(EC)已批准Abecma®(idecabtagene vicleucel;ide-cel)用于治疗成人复发性和难治性癌症患者,这是一项引人瞩目的进展。这一批准为那些先前接受过多种治疗、包括免疫调节剂(IMiD)、蛋白酶体抑制剂(PI)和抗CD38抗体,并在最后一次治疗中表现出疾病进展的难治性多发性骨髓瘤患者带来了新的曙光。本文将探讨Abecma的突破性意义以及对多发性骨髓瘤治疗领域的潜在影响。 Abecma的批准与其治疗范围扩大 Abecma是欧盟批准的第一个嵌合抗原受体(CAR) T细胞免疫疗法,旨在治疗复发性和难治性多发... 查看详情
21
3月
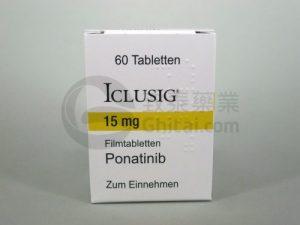
FDA批准普纳替尼ICLUSIG联合化疗治疗费城染色体阳性急性淋巴细胞白血病的补充新药申请
近年来,白血病治疗领域的不断创新与发展为患者带来了新的希望和机遇。费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)作为一种罕见而严重的血液疾病,一直以来都是医学界关注的焦点之一。针对这一病症,医学科学家们不断努力寻找更有效的治疗手段,以提高患者的生存率和生活质量。最近,武田制药宣布,美国食品药品监督管理局(FDA)已批准ICLUSIG(Ponatinib,普纳替尼)的补充新药申请,作为一种联合化疗用于治疗新诊断的Ph+ ALL成年患者。这一批准不仅标志着ICLUSIG在治疗这一疾病领域的重要进展,同时也为患者提供了新的治疗选择。 ICLUSIG联合化疗治疗新诊断Ph+ ALL的临床意义 首个... 查看详情
21
3月
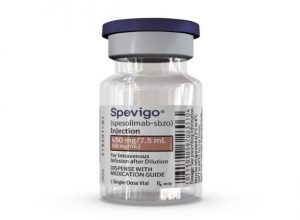
FDA批准Spevigo用于12岁及以上、体重至少40kg的泛发性脓疱型银屑病患者
近日,美国FDA宣布扩大了Spevigo(Spesolimab-sbzo,司柏索利单抗)的批准范围,用于治疗12岁及以上、体重至少40公斤的成人和儿童患者的泛发性脓疱型银屑病(GPP)。这一消息为那些饱受GPP困扰的患者带来了新的希望与治疗选择。 GPP:一种威胁生命的皮肤疾病 泛发性脓疱型银屑病(GPP)是一种潜在威胁生命的中性粒细胞性皮肤病,与普通的银屑病不同,其临床表现更为严重。GPP由中性粒细胞在皮肤中的异常积聚引起,导致全身形成疼痛的无菌脓疱。患者的临床病程各不相同,有些可能伴随着周期性的病情复发,给患者的生活带来极大困扰。 Spevigo:靶向治疗GPP的新药物 Spevigo是由... 查看详情
20
3月
FDA接受酒渣鼻药物DFD-29(盐酸米诺环素缓释胶囊)新药申请
酒渣鼻,或称红斑痤疮,是一种困扰许多人的慢性皮肤问题,尤其好发于颜面中央,给患者带来不少烦恼。针对这一难题,近日,Journey Medical Corporation宣布其研发的新药DFD-29(盐酸米诺环素缓释胶囊)已被美国FDA接受新药申请。若获批准,这将成为治疗酒渣鼻的一项重要里程碑,也将为患者带来全新的治疗选择。 酒渣鼻的挑战与需求 酒渣鼻,作为一种慢性炎症性皮肤病,其临床表现多样,常见于成年人,给患者的外貌和心理健康带来不小影响。目前,酒渣鼻的治疗选择相对有限,且效果不尽如人意。局部治疗如伊维菌素等可以缓解症状,但长期使用可能存在局限性。口服药物方面,目前仅有少数抗生素被批准用于酒... 查看详情
20
3月
美国FDA批准Tryvio(Aprocitentan)用于治疗顽固性高血压
高血压是全球范围内的健康问题,而顽固性高血压更是其中的一大挑战。尽管有多种药物可供选择,但仍有一部分患者难以有效控制血压。然而,一项令人振奋的消息在近期传来:Tryvio(Aprocitentan)口服片剂,由Idorsia与强生联合开发,已经获得美国FDA的批准,用于治疗成年高血压患者。这标志着30年来首个基于新机制的降血压小分子疗法的成功问世,为顽固性高血压患者带来了新的希望。 新药登场:Tryvio(Aprocitentan)的诞生 Tryvio(Aprocitentan)是一款革命性的口服拮抗剂,靶向双重内皮素(Endothelin, ETA/ETB)受体。通过有效抑制ET-1与ETA... 查看详情
20
3月
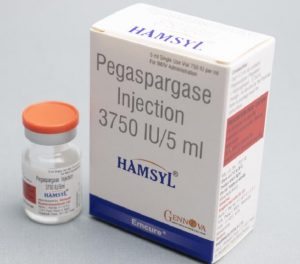
培门冬酶HAMSYL(Pegaspargase)治疗儿童急性淋巴细胞白血病在印度上市
在医学领域,不断的创新和进步为治疗罕见疾病带来新的曙光。2024年3月8日,总部位于浦那的Gennova生物制药宣布推出印度首款儿科包装规格的培门冬酶 HAMSYL Junior(Pegaspargase),标志着为印度儿童急性淋巴细胞白血病(ALL)患者提供医疗服务迈出了重要一步。 开拓创新之路 急性淋巴细胞白血病是一种罕见而具有挑战性的血癌,主要影响儿童。Gennova生物制药自2014年起开始着手解决ALL这一难题,推出了HAMSYL。这种经济实惠且有质量保证的培门冬酶,起初包装尺寸为3750 IU。这项创新不仅支持满足患者需求,还简化了耗时繁琐的进口药物过程,并在抗击ALL的过程中降低... 查看详情
20
3月
FDA批准Lenmeldy(Arsa-cel)用于治疗儿童异染性脑白质营养不良
在罕见遗传疾病领域,医学的进步一直是无比珍贵的。2024年3月18日,美国FDA批准了由Orchard Therapeutics研发的基因疗法Lenmeldy(atidarsagene autotemcel,arsa-cel),用于治疗满足特定条件的异染性脑白质营养不良(MLD)儿童患者。这一里程碑式的批准标志着基因治疗在罕见疾病治疗领域的重大突破,为那些饱受病痛折磨的患者和家庭带来了新的希望。 Lenmeldy的治疗效果 Lenmeldy(atidarsagene autotemcel,arsa-cel)是首个获得FDA批准用于治疗MLD的基因疗法。通过分析数据可以发现,相较于未经治疗的儿童... 查看详情
17
3月
NICE推荐Epcoritamab(Tepkinly/epkinly)用于B细胞淋巴瘤患者
2024年3月,国家卫生与护理卓越研究所(NICE)做出了一项具有里程碑意义的决定,正式推荐Epcoritamab(Tepkinly/epkinly)用于治疗成年复发性或难治性弥漫性大B细胞淋巴瘤(DLBCL)患者,这是一种在接受两种或两种以上先前系统性治疗后的疾病。这一重要推荐标志着我们在与最具侵略性的淋巴瘤之一的斗争中迈出了一大步,为那些已经耗尽其他治疗选择的患者带来了新的希望。 DLBCL以其快速进展和具有挑战性的治疗格局而闻名,这已经让许多患者及其医疗保健提供者急需创新的治疗选择。Epcoritamab(Tepkinly/epkinly),一种新型的治疗药物,已经成为希望的象征,根据N... 查看详情
16
3月
FDA批准XHANCE(丙酸氟替卡松鼻喷雾剂)用于治疗成人慢性鼻窦炎
在耳鼻喉(ENT)和过敏治疗领域,新的希望正在为成人患者带来解决方案。近日,Optinose制药公司宣布,他们的创新药物XHANCE®(fluticasone propionate)丙酸氟替卡松鼻喷雾剂已经获得美国食品和药物管理局(FDA)的批准,用于治疗18岁及以上患者的慢性鼻窦炎,而这些患者并不伴有鼻息肉。这一突破性的批准为患者和医生提供了新的治疗选择,有望改善他们的生活质量。 XHANCE的作用机制 XHANCE的批准源于ReOpen计划的数据,该计划对XHANCE治疗成人慢性鼻窦炎的疗效进行了评估。与传统鼻喷雾剂不同的是,XHANCE是一种药物-设备组合产品,它将临床上广泛使用的鼻类固... 查看详情
15
3月
FDA批准Breyanzi(liso-cel)用于复发或难治性慢性淋巴细胞白血病和小淋巴细胞淋巴瘤
慢性淋巴细胞白血病(CLL)和小淋巴细胞淋巴瘤(SLL)是两种严重的血液恶性肿瘤,患者往往在复发或难治性阶段面临治疗挑战。然而,随着科学技术的进步,特别是CAR T细胞疗法的崛起,治疗前景正在发生改变。最近,美国食品药品监督管理局(FDA)加速批准了Breyanzi(Lisocabtagene Maraleucel,简称liso-cel;商品名Breyanzi),作为一种新的CAR T细胞疗法,用于治疗复发/难治性CLL或SLL。这一决定标志着对于这些患者而言,治疗选择的范围进一步扩大,为患者带来了新的曙光。 临床试验数据 Breyanzi的加速批准基于来自于TRANSCEND CLL 004... 查看详情