11
6月
Arexvy疫苗用于50-59岁高危成人预防呼吸道合胞病毒感染
2024年6月7日,葛兰素史克(GSK)宣布了一项重大突破,美国食品药品监督管理局(FDA)批准了其重组呼吸道合胞病毒(RSV)疫苗Arexvy的适用范围扩展至50-59岁的高危成人。这一消息不仅为广大中年群体带来了福音,也标志着RSV防治进入了一个新的阶段。本文将详细探讨这一扩展背后的研究成果、Arexvy疫苗的作用机制及其在全球范围内的影响。 I. Arexvy疫苗的研发背景及重要性 1.1 呼吸道合胞病毒(RSV)简介 呼吸道合胞病毒(RSV)是一种极具传染性的病毒,主要影响肺部和呼吸道。特别是对于免疫功能低下、高龄或患有合并症的成人,RSV感染的风险显著增加。感染RSV后,患者可能会出... 查看详情
11
6月
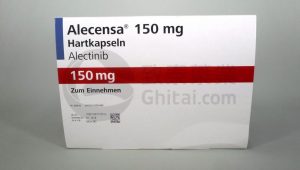
Alecensa(阿来替尼)在欧盟获批用于术后辅助治疗ALK阳性非小细胞肺癌
肺癌是全球范围内癌症死亡的主要原因之一,每年导致约180万人死亡,相当于每天有4900多人死于该疾病。在所有类型的肺癌中,非小细胞肺癌(NSCLC)是最常见的一种,占据了所有病例的85%。尽管在早期阶段进行手术和辅助化疗,但约45%到76%的患者仍会经历癌症复发,这意味着在肺癌扩散之前尽早进行有效的治疗是至关重要的。2024年6月10日,罗氏公司宣布,欧盟委员会已批准Alecensa(alectinib,阿来替尼) 单药作为术后辅助治疗,用于复发风险较高的间变性淋巴瘤激酶 (ALK) 阳性非小细胞肺癌 (NSCLC) 成年患者。这一批准标志着Alecensa(阿来替尼)在治疗ALK阳性早期肺癌... 查看详情
08
6月
FDA批准RYTELO(Imetelstat)用于治疗患有输血依赖性贫血的低风险骨髓增生异常综合症患者
在现代医学的不断进步中,癌症和血液病的治疗取得了显著的突破。近期,美国食品药品监督管理局(FDA)批准了Geron Corporation开发的RYTELO™(Imetelstat),用于治疗低风险骨髓增生异常综合症(LR-MDS)患者的输血依赖性贫血。这一批准不仅标志着一种全新治疗手段的诞生,还为无数患者带来了新的希望。 RYTELO的批准与临床试验成果 临床试验背景 RYTELO的获批是基于《柳叶刀》上发表的IMerge 3期临床试验结果。此次试验包括了大量患有输血依赖性贫血的低至中等-1风险骨髓增生异常综合症(MDS)的成年患者。这些患者在试验中需要每八周至少输注4个或更多的红细胞单位,... 查看详情
07
6月
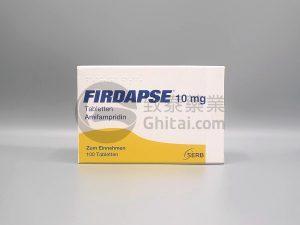
FDA批准增加Firdapse(阿米吡啶)治疗Lambert-Eaton肌无力综合征的最大每日剂量
Catalyst制药公司近日宣布了一个重大的进展,美国食品药品监督管理局(FDA)已批准了Firdapse(阿米吡啶)的补充新药申请(sNDA)。这一批准标志着在治疗Lambert-Eaton肌无力综合征(LEMS)方面的一个重要里程碑,特别是通过增加每日最大总维持剂量,为医疗保健提供者和患者提供了更多的治疗方案灵活性。 1. FDA批准的新变更 根据Catalyst制药公司5月30日发布的新闻稿,FDA已批准Firdapse的补充新药申请,显著增加了该药物用于治疗LEMS的每日最大总维持剂量。这一变更不仅提升了药物使用的灵活性,还为不同体重和年龄段的患者提供了更为有效的治疗方案。 1.1 成... 查看详情
07
6月
欧盟CHMP推荐批准rADAMTS13用于罕见凝血障碍
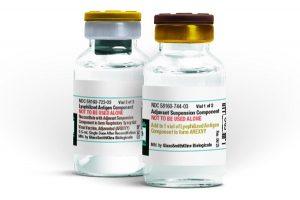
近日,武田公司宣布,其研发的重组ADAMTS13酶(rADAMTS13)获得了欧洲药品管理局(EMA)人类药物委员会(CHMP)的推荐批准。这一新药有望为治疗先天性血栓性血小板减少性紫癜(cTTP)的儿童和成人带来福音。 先天性血栓性血小板减少性紫癜的概述 什么是cTTP? 先天性血栓性血小板减少性紫癜(cTTP)是一种极其罕见且严重的凝血障碍。这种疾病属于血栓性血小板减少性紫癜(TTP)的遗传形式,占TTP患者的比例不超过5%。cTTP的病因是由于体内缺乏ADAMTS13酶,这种酶负责裂解血管性血友病因子(VWF)。当ADAMTS13酶不足时,超大VWF多聚体在血液中积累,导致血小板异常聚集... 查看详情
07
6月
Durveqtix获得欧洲药品管理局有条件上市许可用于治疗血友病B成人患者
近日,欧洲药品管理局(EMA)建议授予辉瑞研发的Durveqtix(fidanacogene elaparvovec)有条件上市许可,用于治疗重度和中重度血友病B的成人患者。这个决定标志着基因疗法在血友病治疗中的重要突破。 血友病B:危及生命的退行性疾病 疾病背景 血友病B是一种由基因突变引起的罕见遗传性出血性疾病,导致患者缺乏凝血因子IX(FIX)。这种缺陷使患者容易发生自发性出血,特别是在关节、肌肉和内脏器官中,引起严重的疼痛、肿胀和关节损伤。如果不加以控制,频繁的出血事件可能会导致慢性关节病变和其他严重并发症。 现有治疗方法的局限性 目前,血友病B的标准治疗方法之一是因子替代疗法。这种疗... 查看详情
04
6月
贝伐单抗生物类似药物Avzivi获得欧洲药品管理局肯定的积极意见
欧洲药品管理局人用药品委员会(CHMP)已对生物类似药物Avzivi采取了积极意见,这是一种单克隆抗体,参照生物制剂贝伐单抗(Avastin)。该建议现已提交给欧洲委员会,后者将决定是否授予该生物类似药物在结肠或直肠癌、乳腺癌、非小细胞肺癌(NSCLC)、肾细胞癌、上皮性卵巢输卵管或原发性腹膜癌以及子宫颈癌患者治疗的上市许可。如果获批,该药将作为25毫克/毫升的浓缩注射液供应。 Bio-Thera Solutions首席执行官李胜锋在一份新闻发布中表示:“Bio-Thera致力于开发高质量的生物类似药物,以扩大患者获取重要治疗药物如贝伐单抗的机会。”“Avzivi获得积极的CHMP推荐意见表明... 查看详情
03
6月
FDA批准mRESVIA疫苗用于预防呼吸道合胞病毒(RSV)感染
2024年5月31日,Moderna公司在马萨诸塞州剑桥宣布了一项重大消息:美国食品和药物管理局(FDA)已经批准他们开发的呼吸道合胞病毒(RSV)mRNA疫苗mRESVIA(mRNA-1345)上市。这款疫苗旨在保护60岁及以上成年人免受RSV感染引起的下呼吸道疾病(RSV-LRTD)。这一批准标志着Moderna公司迈出的又一重要步伐,成为继其COVID-19 mRNA疫苗之后的第二项获批疫苗。 里程碑:mRESVIA的诞生 mRESVIA是首款以单剂量预充式注射器供应的RSV疫苗,其研发历经艰辛但也凝聚了现代医学科技的精华。 该疫苗的批准主要基于一项名为ConquerRSV的3期临床试验... 查看详情
03
6月
FDA同意优先审查Zanidatamab用于治疗HER2阳性胆道癌
爵士制药公司(JAZZ)近日发布的消息引起了医学界的广泛关注。根据5月29日的新闻稿,美国食品药品监督管理局(FDA)已同意优先审查Zanidatamab用于治疗既往治疗过的、不可切除的、局部晚期或转移性HER2阳性胆道癌(BTC)的生物制剂许可申请。这一消息给患有这一罕见病症的患者带来了新的曙光,也为医学界带来了新的希望。 胆道癌的挑战与需求 胆道癌,又称胆管癌,是一种罕见但危害巨大的癌症类型,它在胆管中形成,连接着肝脏、胆囊和小肠,给患者带来了严重的身体不适。这种疾病的主要症状包括肝功能异常、腹痛、黄疸、体重减轻等,常常在晚期才被诊断出来,给治疗带来了极大的挑战。当前对于胆道癌的治疗选择十... 查看详情
03
6月
Austedo XR获得FDA批准用于治疗迟发性运动障碍和亨廷顿病
近日,Teva制药公司宣布其新药Austedo XR已获得美国食品药品监督管理局(FDA)的批准,推出多种新剂量。Austedo XR是一种专门用于治疗迟发性运动障碍(TD)和亨廷顿病相关舞蹈症(HD)的药物,其新的剂量强度将为患者提供更多的治疗选择。这一消息不仅标志着在这些疾病治疗领域的一大进步,也为广大患者带来了新的希望。 Austedo XR的新剂量选择 四种新剂量的推出 Austedo XR现在提供四种新的片剂强度:30毫克、36毫克、42毫克和48毫克。这些新剂量的推出使得药物的使用更加灵活和个性化。此前,该药物仅提供6毫克、12毫克和24毫克三种剂量。新的剂量选择将有助于医生根据患... 查看详情