鲁索替尼Jakavi治疗骨髓纤维化和贫血患者的新型给药策略的有效性和安全性
贫血是骨髓纤维化 (MF) 的常见表现,贫血的 MF 患者对有效治疗的需求尚未得到满足。REALIZE 2 期研究 (NCT02966353) 评估了一种新型鲁索替尼Jakavi给药策略的有效性和安全性,该策略在贫血 MF 患者中降低起始剂量并延迟滴定。51 名原发性 MF (66.7%)、特发性血小板增多症 MF (21.6%) 或真性红细胞增多症后 MF (11.8%) 患者有可触及的脾肿大和血红蛋白 <10 g/dl。中位年龄为 67 (45-88) 岁,41.2% 为女性,18% 为输血依赖性。患者在前 12 周接受 10 mg ruxolitinib 两次,然后根据疗效和血小板计数,允许滴定至 25 mg 两次。全面的,在研究期间的任何时间,70% 的患者可触及的脾脏长度减少了 ≥ 50%。导致剂量中断/调整的最常见不良事件是血小板减少症 (17.6%) 和贫血 (11.8%)。增加剂量的患者在基线时具有更大的脾脏大小和更高的白细胞计数。与基线相比,中位血红蛋白水平保持稳定,输血需求没有增加。这些结果强化了这样的观点,即没有必要因为共存或治疗中出现的贫血而延迟或停用鲁索替尼Jakavi。与基线相比,中位血红蛋白水平保持稳定,输血需求没有增加。这些结果强化了这样的观点,即没有必要因为共存或治疗中出现的贫血而延迟或停用鲁索替尼Jakavi。与基线相比,中位血红蛋白水平保持稳定,输血需求没有增加。这些结果强化了这样的观点,即没有必要因为共存或治疗中出现的贫血而延迟或停用鲁索替尼Jakavi。
芦可替尼(捷恪卫,鲁索替尼,Jakavi)
目录
介绍
骨髓纤维化 (MF) 是一种血液肿瘤,其特征是 Janus 激酶 (JAK)/信号转导和转录激活因子 (STAT) 信号通路失调,参与正常造血、细胞生长和免疫功能。 MF 的主要特征包括非典型巨核细胞形态、骨髓纤维化、贫血、脾肿大、疲劳、体重减轻、盗汗和进展为急性髓系白血病的风险。由于年龄限制及其相关的高死亡率,同种异体干细胞移植是 MF 唯一可能治愈的治疗方法,实际上只能应用于少数患者 。MF 的其他可用治疗旨在缓解症状,包括脾肿大、贫血、全身症状、骨痛和症状性髓外造血。
大多数 MF 患者表现为轻度至中度贫血,并随着疾病的进展而恶化。MF 的贫血部分是由于红细胞生成减少,但也可能因脾功能亢进、炎性细胞因子的影响以及铁、叶酸或维生素 B12 缺乏、胃肠道出血等并发原因而加重,或者更罕见,免疫溶血。贫血是用于诊断原发性 MF (PMF)、真性红细胞增多症后 MF (PPV-MF) 和原发性血小板增多症 MF (PET-MF)的标准,并且是一个重要因素在风险评估中,赋予不利的预后影响。目前治疗 MF 贫血的方法包括雄激素、促红细胞生成素、免疫调节剂(沙利度胺、来那度胺)和泼尼松。然而,这些药物可能并非对所有患者都有效,并且可能会出现导致停药的副作用。例如,促红细胞生成素很少对依赖输血 (TD) 的患者起作用,约占 MF 患者的 25%。因此,需要新的方法来管理 MF 贫血患者。从这个意义上说,正在探索多种治疗骨髓纤维化贫血的研究疗法,包括 luspatercept 和莫罗替尼。
Ruxolitinib 是一种有效的 JAK1/JAK2 抑制剂,被批准用于治疗成人 PMF、PPV-MF 或 PET-MF的 MF 相关脾肿大或症状。根据血小板计数(≥50 至 <100 × 10 9 /l、100 至 200 × 10 9 /l、>200 × 10 9 /l ),推荐的起始剂量为 5、15 或 20 mg 每天两次(bid), 分别) 无论基线时的血红蛋白 (Hb) 水平如何 。剂量依赖性贫血已经观察到与鲁索利替尼治疗,与Hb水平开始治疗,并通过第24周[恢复到基线后达到8和12周之间的最低点]。这种贫血通常与剂量减少和/或输血,不象MF的贫血,贫血管理而在鲁索利替尼治疗并不总生存[不利地影响]。在 MF 中使用鲁索替尼Jakavi的临床经验表明,使用较低的起始剂量 10 mg 每天两次并逐渐滴定可以减少治疗相关性贫血的影响,同时保持已经出现贫血的患者的治疗反应。这种方法假设从较低剂量开始可能会通过降低 JAK 介导的造血抑制水平来改变初始 Hb 下降的速度和最低点。
为了测试这一提议的替代给药实践的价值,我们进行了 REALIZE 开放标签、单臂、2 期研究,该研究评估了鲁索替尼Jakavi新给药策略的有效性和安全性,包括降低起始剂量(10 毫克每天两次) ) 在 MF 和贫血患者 (Hb <10 g/dl) 中延迟滴定 。
芦可替尼(捷恪卫,鲁索替尼,Jakavi)
材料和方法
REALIZE 研究是一项 2 期、开放标签、单臂研究,在欧洲、亚洲和北美的 20 个中心进行,旨在评估鲁索替尼Jakavi替代给药策略在治疗贫血 MF 患者中的有效性和安全性。该方案在每个研究地点得到了适当的独立审查委员会/独立伦理委员会/研究伦理委员会的批准,并且所有患者都提供了书面知情同意书。
如果患者患有 PMF、PET-MF 或 PPV-MF,则他们有资格参加;年龄≥18岁;可触及脾脏(左肋缘下≥5 cm,在安静呼吸时使用软尺测量);Hb 水平 <10 g/dl;东部肿瘤合作组 (ECOG) 表现状态为 0、1 或 2;和外周血原始细胞<10%。PMF根据2016修订版国际标准诊断,PPV-MF或PET-MF根据标准诊断],无论 JAK2 突变状态如何。在进入研究之前,排除了贫血的共存原因,如铁、叶酸或维生素 B12 缺乏,以及门脉高压性高血压胃病引起的胃肠道出血。要求有红细胞输血史的患者在基线前 12 周内有记录在案的输血记录。根据骨髓增殖性肿瘤研究和治疗国际工作组 (IWG MRT) 的标准,输血依赖被定义为在基线前 12 周内输血 6 次或更多次。
排除标准包括:先前用任何 JAK1 或 JAK2 抑制剂治疗;基线访视时骨髓储备不足,表现为以下至少一项:绝对中性粒细胞计数 (ANC) ≤1 × 10 9 /l,血小板计数 <50 × 10 9/l,没有生长因子、血小板生成因子或血小板输注的帮助,尽管输血,Hb ≤ 6.5 g/dl;肾功能严重受损(定义为肌酐清除率低于 30 毫升/分钟);肝功能不足(总胆红素≥2.5×正常上限[ULN],随后测定直接胆红素≥2.5×ULN或丙氨酸氨基转移酶>2.5×ULN或天冬氨酸氨基转移酶>2.5×ULN);在筛选时与强效全身抑制剂或 CYP3A4 诱导剂同时治疗;急性病毒性肝炎或活动性慢性乙型或丙型肝炎感染或进行性多灶性白质脑病史。除了接受治疗的早期鳞状细胞癌或基底细胞癌外,过去 3 年内有恶性肿瘤病史的患者也被排除在外。
治疗
符合条件的患者在治疗的前 12 周接受 10 mg 口服剂量的鲁索替尼Jakavi,无论其基线时的血小板计数如何,之后根据血小板计数和疗效,允许滴定至多 25 mg 每天两次(图 2)。 )。ANC >0.5 × 10 9 /l 和 Hb ≥6.5 g/dl 的患者有资格增加剂量。血小板计数≥100 × 10 9 /l 至≤200 × 10 9 /l 的患者,目标剂量为 12 周 15 mg每天两次;对于血小板计数≥200 × 10 9 /l 的患者,从 16 周开始服用 20 mg 每天两次;从第 20 周起,允许血小板计数≥200 × 10 9 的患者服用 25 mg 每天两次/l 可触及的脾脏长度 (SL) 未减少 50%。对于那些 SL 从基线降低 50% 以上的患者,剂量增加是可选的。只要研究治疗有益,患者就会接受研究治疗,直至最后一位患者首次治疗后 48 周。
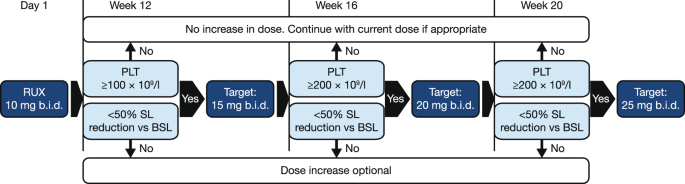
每天两次bid,BSL基线脾脏长度,PLT血小板,RUX ruxolitinib,SL脾脏长度。
终点和评估
主要终点是第 24 周 SL 降低≥50% 的患者比例。次要终点包括输血要求、安全性(不良事件 [AE])、Hb 变化和患者报告的结果。疗效评估包括:SL、随着时间的推移输血,以及由 7 分 MF 评分 (MF-7)、MF 症状评估表 (MFSAF) 2.0 版和患者总体变化印象 (PGIC) 评估的患者报告结果)。终点通过基线时的输血依赖性状态进行评估,如先前定义的 。
安全性评估包括 AE、血液血液学值和血液生化参数。
统计分析
全分析集和安全集相同。分类数据以频率和百分比表示。对于连续数据,使用平均值、标准偏差、中位数、第 25 和第 75 个百分位数、最小值和最大值。
对研究治疗的主要疗效的评估是基于对第 24 周观察到的 SL 反应患者比例的计算及其使用β-二项式模型的后验分布。使用 Clopper 和 Pearson 精确方法评估第 48 周的脾缓解率,作为第 48 周可触及 SL 减少≥50% 的患者比例的点估计值以及相应的精确 95% 置信区间 (CI)。
结果
研究中共有 51 名患者接受治疗,其中 50 名在数据截止日期 2019 年 2 月 16 日之前已完成或停止治疗。患者的中位年龄为 67(范围 45-88)岁,约 2 -三分之一的患者患有 PMF。大多数患者患有动态国际预后评分系统 (DIPSS) 中级 1 或中级 2 疾病(分别为 9 [17.6%] 和 28 [54.9%]),并且 10 (19.6%) 被归类为 DIPSS 高危。在基线时,9 名患者为 TD,41 名患者为非 TD(非 TD)。11 名患者在基线时血小板计数<100 × 10 9 /l。
共有 28 名 (54.9%) 患者完成了研究,1 名患者在数据截止时被视为正在进行治疗。停止治疗的原因包括:患者决定(13.7%;n = 7,包括:个人原因,n = 2;造血干细胞移植,n = 2;撤回同意,n = 2;以及难以遵守协议——所需的 就诊时间表,n = 1),医生决定(5.9%;n = 3,包括造血干细胞移植,n = 2,对治疗无反应,n = 1),AE(7.8%;n = 4),死亡 (7.8%; n = 4)、疾病进展 (3.9%; n = 2) 或方案偏差 (3.9%; n = 2)。
加药
在研究期间,鲁索替尼的中位日剂量为 20(范围 8-36)mg,中位暴露时间为 62.6(范围 3-92)周。到第 24 周,26.2%(11/42 名患者)接受的每日总剂量≥30 mg,到第 48 周,有剂量数据的 37 名患者中有 12 名(32.4%)接受了每日 30 mg 或更多的剂量(图 2)。。在最终数据截止时,12.0% (6/50) 的患者接受了剂量增加,30.0% (15/50) 的患者维持了其起始剂量。大多数维持起始剂量的患者在第 12 周或更晚(11/15 名患者)实现了 ≥ 50% 的脾脏长度减少,2 名患者在第 12 周第一个方案要求增加剂量之前停止治疗。
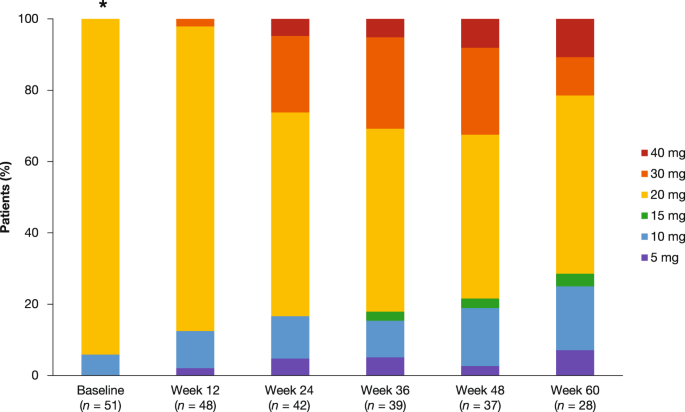
如下达到每日总剂量:5mg qd;5毫克出价;5 毫克 qd 和 10 毫克 qd; 10 毫克出价; 15毫克出价;每天两次 20 毫克出价; qd每天一次。*三名患者以 10 毫克 qd 开始研究。其中两个是在 5 天和 6 天内纠正的剂量错误。第三个是医生对因疾病进展而未继续进行下一阶段研究且未包括在后续分析中的患者的决定。
功效
到第 24 周,共有 56%(95% CI 41.3–70.0;n / N = 28/50)的患者的 SL 减少了 ≥ 50%。在基线时为 TD 的 9 名患者中有 6 名(66.7%)符合SL 降低≥50% 的主要终点,40 名基线非 TD 患者中有 21 名 (52.5%) 达到该终点。当按 DIPSS 状态分层时,55.6% (5/9) 的中间 1 风险、57.1% (16/28) 的中间 2 风险和 40% (4/10) 的高风险患者达到 ≥ 50%到第 24 周时 SL 减少。总共有 70% (35/50) 的患者在研究期间的任何时间都实现了 SL 减少 ≥ 50%(图 3A)。
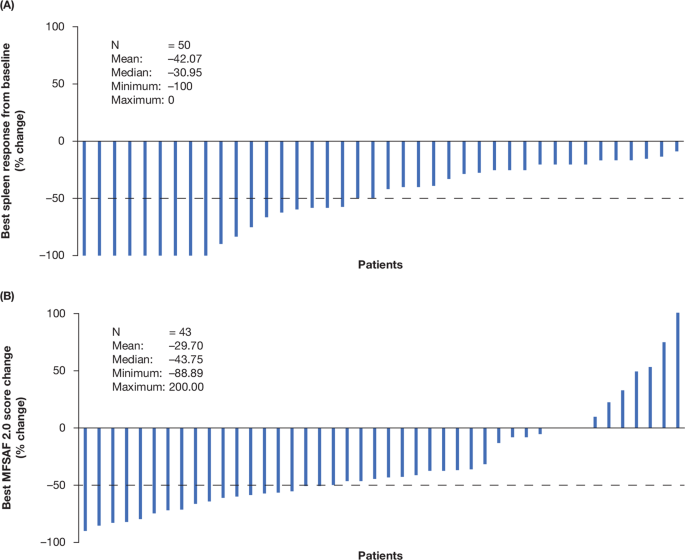
根据个体患者的脾脏长度 ( A ) 和 MFSAF 评分变化 ( B ) 的最佳反应。注意:患者 44 获得了 +200.7% 的最佳 MFSAF 评分。MFSAF 骨髓纤维化症状评估表。
在研究期间增加剂量的患者的基线特征通常与没有增加剂量的患者相似。然而,与患者相比,接受剂量增加的更大比例的患者具有更大的可触及脾脏长度(中位数 14 cm 对 9 cm)和更高的中位数白细胞计数(14 × 10 9 /l 对 8.7 × 10 9 /l)谁没有接受剂量增加。此外,未接受剂量增加的患者血小板计数低的发生率较高(27.8% 对 6.7%)。在第 12 周时接受剂量增加的 15 名患者中,7 名 (47%) 在第 24 周时脾脏大小减少≥50% 并且是脾脏反应者。
患者报告的结果
在第 24 周,MF-7 总症状评分 (TSS) 相对于基线的中位百分比变化为 -54.5%(范围:-100.0% 至 +150.0%),中位绝对变化为 8 分,到第 48 周,与基线相比的中位数百分比变化为 -42.3(范围:-100.0% 至 +100.0%),中位数绝对变化为 4 分(补充图 S 1)。分数从 0(不存在)到 10(可想而知的最差),因此分数降低表示症状有所改善。按风险组进行评估时,分别占中 1 级风险、中级 2 风险和高风险 DIPSS 组的 75.0% (6/8)、84.6% (22/26) 和 75.0% (6/8) ,报告在研究期间的任何时间点 MF-7 TSS(症状改善)减少≥50%。在修改后的 MFSAF 2.0 版 TSS 中也观察到了类似的变化,在研究期间任何时间与基线相比的最大中值变化为 -43.8%(范围:-88.9% 至 +200.0%)(图 3B))。在第 24 周,MFSAF 评分相对于基线的中位百分比变化为 –55.2%(范围:-100.0% 至 +145.5%),中位绝对变化为 9 分,到第 48 周,相对于基线的中位百分比变化为-45.5(范围:-100.0% 至 +100.0%),中位数绝对变化为 7.5 分(补充图 S 2)。对于根据风险组的 MFSAF 评分,中 1 级风险、中级 2 和高风险 DIPSS 组的 75.0% (6/8)、84.6% (22/26) 和 50.0% (4/8)分别报告了研究期间任何时间点的评分降低 ≥ 50%。使用 PGIC 评分,共有 82.9% (34/41) 的患者在第 24 周和 87.9% (29/33) 报告在第 48 周有所改善(补充图 S 3)。
安全
总体而言,44/51 受试者 (86.3%) 报告了至少 1 次任何级别的 AE,26/51 (51.0%) 被认为与治疗相关。五名患者经历了导致治疗中断的 AE:贫血恶化(3 级);白细胞增多症(3 级);克罗恩病再激活(4 级);细菌性下呼吸道感染(5级);和败血症(4 级)。总共有 25 名 (49.0%) 患者至少减少了 1 次剂量,16 名 (31.4%) 患者至少中断了 1 次剂量(图 2)。AE 是减少剂量和中断剂量的最常见原因。导致剂量中断/调整的最常见 AE 是血小板减少症(17.6% [9/51] 患者)和贫血(11.8% [6/51] 患者),这也是整个研究人群中最常见的 AE。在研究期间,1 名患者发生血栓事件(动脉视网膜血栓形成),另一名患者进展为急性髓系白血病。
总共有 8 名患者死亡,其中 7 名死亡发生在研究或研究安全随访期间。死亡的主要原因是:感染和侵染 ( n = 4)、心力衰竭 ( n = 1)、大肠杆菌引起的败血症背景下的多器官功能障碍综合征( n = 1),以及 MF 进展为急性髓系白血病( n = 1)。其中,4 名患者因 AE 停止治疗。与先前在 MF 中使用鲁索替尼的试验相比,在 REALIZE 试验中未观察到新的 AE 。
血红蛋白水平和血小板计数的变化
在 82.4% (42/51) 的患者中观察到 Hb 降低,其中 54.9% (28/51) 为 3 级。 在 Hb 降低 3 级的患者中,1 名患者进入试验时 Hb 计数降低为 1 级23 名和 4 名患者分别以 2 级或 3 级 Hb 计数降低进入试验。在整个研究过程中,Hb 中值水平保持稳定,并根据需要支持红细胞 (RBC) 输血(图 4A))。66.7% (34/51) 的患者(17.6% [9/51] 3 或 4 级)出现血小板减少。在 3 级血小板减少的 6 名患者中,4 和 2 名分别以 1 级或 2 级血小板计数减少进入试验,在 3 名血小板减少 4 级患者中,2 和 1 名进入试验1 级或 2 级分别减少血小板计数。在研究期间,共有 11.8% (6/51) 的患者需要输注血小板。在基线后初始下降后,在整个研究过程中,那些仍在接受研究的患者的中位血小板计数保持稳定(图 4B)。在研究过程中接受剂量增加的患者和未接受剂量增加的患者之间的血小板计数和血红蛋白水平相似(补充图 S4)。
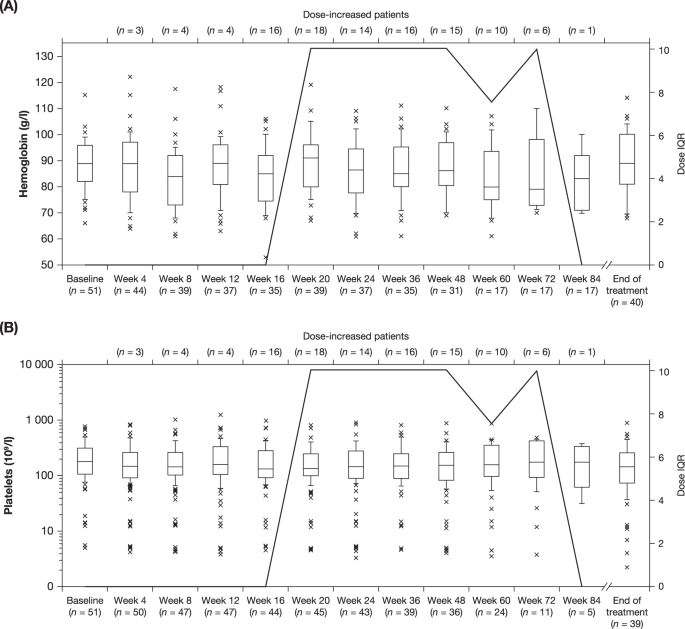
随着时间的推移,中位血红蛋白 ( A ) 和血小板 ( B ) 水平。方框表示第 25-75 个百分位数,中位日剂量表示为水平线。胡须表示第 10-90 个百分位数。不显示超出此范围的值。X 标记表示高于 Q3 的 IQR 的 1.5 倍和低于 Q1 的 IQR 的 3 倍。实线表示每日总剂量自起始剂量变化的 IQR。IQR四分位距,Q1第一四分位数;Q3 第三个四分位数。
输血要求
在研究期间,66.7% (34/51) 的患者接受了所有输血成分(全血输血、浓缩红细胞输血和血小板输血)。在研究期间接受促红细胞生成素治疗的 8 名患者中,有 6 名在研究前开始;1 名患者在研究前接受促红细胞生成素治疗,但在研究开始后停药。此外,根据医生的决定,11 名患者在研究期间接受了低剂量皮质类固醇,通常是在手术期间或作为术前用药的单剂量。TD 患者在前 4 周内接受的 RBC 单位平均数在基线时最高,约为 3.8 个单位,直到第 48 周左右下降到 0.5 和 1.8 个单位之间,然后进一步下降到 <1 个单位/4 周前随后的访问(图 5A)。基线前 4 周非 TD 患者的平均 RBC 单位较低,约为 0.5 单位,并保持在 0.5 和 1.0 单位之间,直到第 36 周,之后平均值下降至 <0.3 单位/4 周(图 5A) . 如图 5A 所示,总体而言,TD 患者对 RBC 输血的需求降低,并且在整个研究中对非 TD 患者保持相似水平。在达到和未达到脾反应的患者中,输血需求都有减少的趋势(图 5B)。基线时为 TD 但没有脾反应的患者显示出红细胞输血需求减少的趋势(补充图 S 5A)。根据剂量增加的 RBC 输血显示在补充图 S 5B 中。
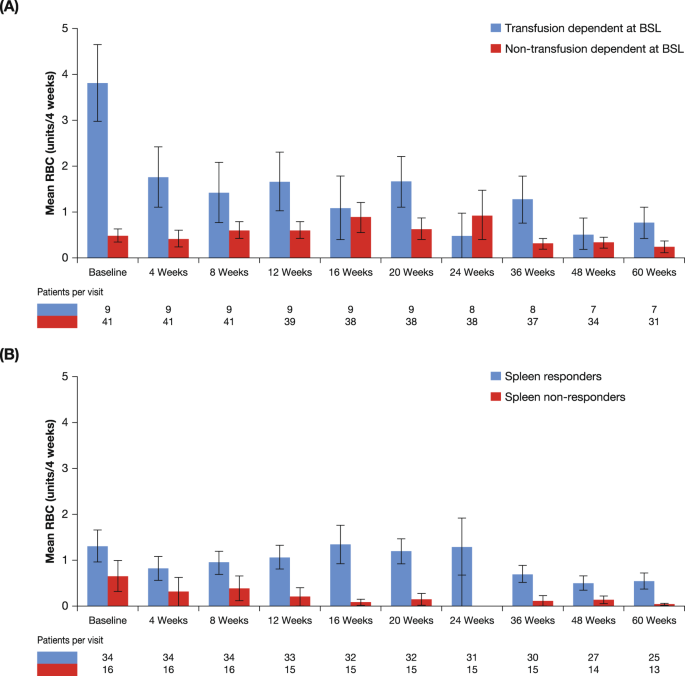
研究期间在基线时依赖输血或不依赖输血的患者 ( A ) 和研究期间任何时间的脾响应者和非响应者 ( B ) 中接受的 RBC 单位平均数。BSL 基线脾脏长度;红细胞红细胞。
讨论
贫血是MF的常见表现。其目前的治疗方法包括雄激素、红细胞生成刺激剂 (ESA)、免疫调节剂如沙利度胺和来那度胺以及泼尼松 ,但它们对许多患者无效,尤其是对输血依赖者。因此,需要针对MF患者贫血的新疗法。Luspatercept 是一种缓解红细胞生成末期阻断的药物,在低风险骨髓增生异常综合征的贫血中显示出疗效,并在 MF 贫血患者的 2 期临床试验中显示出有希望的结果并正在与 ruxolitinib 联合进行 3 期研究。此外,在最近的一项 2 期试验中,JAK1/JAK2 抑制剂莫洛替尼已显示出对 MF 贫血的疗效,目前正在进行一项比较该药物与达那唑的 3 期试验。
ruxolitinib 是一种有效的 JAK1/JAK2 抑制剂,被批准用于治疗 MF 相关的脾肿大或症状,可能与剂量依赖性贫血有关,大多数出现在治疗的前 12 周。必须指出的是,使用 ruxolitinib 的患者通常耐受甚至非常低的 Hb 水平,这可能与炎性细胞因子水平升高导致贫血耐受性较差的事实有关。然而,总体而言,鲁索替尼治疗下的贫血对部分 MF 患者构成了临床问题。鲁索替尼在 MF 中的临床经验表明,较低的起始剂量 10 mg 每天两次并根据血液参数递增滴定可能会降低治疗相关性贫血的影响,同时保持治疗反应 。在此背景下,REALIZE 研究旨在评估鲁索替尼在严重贫血的 MF 患者中的新型给药策略。该方案包括减少初始 ruxolitinib 剂量并在 12 周时评估反应,以便在反应不令人满意且血小板计数保持超过 100 × 10 9 时应用剂量递增/升。总体而言,如果必要和可能,10 mg 每天两次的起始剂量并在治疗 12 周后逐渐递增,对于 MF 贫血患者(包括 TD 患者)是有效且耐受良好的。值得注意的是,由于反应不足而在治疗 12 周时接受剂量增加的患者中,几乎有一半随后达到了脾脏反应。ruxolitinib 1-2 期试验首次强调了接受滴定剂量≥10 mg 每天两次的患者有更高反应率的趋势。虽然这项研究证实了剂量-反应关系,但在独立研究中也观察到 10 mg 每日两次剂量在减少 MF 相关脾肿大和症状方面的功效 。此外,采用这种新的给药策略,尽管基线时存在贫血,但研究中的大多数患者的脾肿大显着减少,MF 相关症状和患者报告的结果有所改善。这些结果与鲁索替尼 3 期研究 和 COMFORT 试验汇总数据分析中报告的结果相当。这些研究表明,基线时贫血的患者和在 ruxolitinib 治疗期间出现贫血的患者与接受比较剂、最佳可用治疗的患者相比,均具有生存优势。
使用 REALIZE 研究中使用的替代给药策略,在第 24 周观察到贫血患者的脾脏反应,无论是否依赖输血。TD 患者的 RBC 输血次数减少,但在非 TD 患者中保持相对一致。Hb 水平在整个研究过程中保持相当稳定,并根据需要提供 RBC 输血支持。如前所述,它已经在临床试验中看到在鲁索替尼治疗的头几个月,MF 患者经常表现出贫血加重,而后来 Hb 水平往往略有改善或恢复到基线值。这可能部分反映了高危患者的剂量减少或提前停药。减少输血负担可能归因于与抑制细胞因子相关的整体性能状态的改善。鲁索替尼治疗后脾肿大的减轻也可能有助于改善贫血。此外,从较低的鲁索替尼剂量开始可能通过降低 JAK 介导的造血抑制水平来改变 Hb 下降和最低点的速度。关于其他副作用,鲁索替尼耐受性良好,未发现新的安全信号。
本研究中的一些患者在鲁索替尼治疗期间接受了 ESA。在 COMFORT-2 研究的事后分析中,在研究期间由治疗医师决定接受 ESA 治疗的 13 名患者中,7 名患者的 Hb 值有所改善,6 名患者中有 2 名在开始时依赖输血ESA 治疗减少了所需的浓缩红细胞输血次数,但不会变得独立于输血 。因此,难以确定 ESA 治疗对本研究中该亚组患者贫血进展的可能影响。
本研究的两个基线特征,从诊断到开始或 ruxolitinib 治疗的时间(中位数 14.9 个月)和在 ruxolitinib 之前接受替代治疗的患者(28/51 患者),可能表明存在延迟 ruxolitinib 治疗开始的趋势,或者它不是在可能需要治疗的患者中考虑首选治疗。在接受过先前治疗的 28 名患者中,21 名在鲁索替尼之前接受了羟基脲。在这种情况下,JUMP 试验的亚组分析(其中 38% 为贫血)的证据支持快速开始 ruxolitinib 治疗,其中预测接受 ruxolitinib 作为一线治疗的患者有更好的脾脏反应 。
基于这些结果,我们建议这种新的给药策略可能适用于因脾肿大和/或 MF 相关症状而开始接受鲁索替尼治疗的 MF 患者,这些患者具有临床相关的贫血(Hb < 10 g/dl)。多项研究的数据表明,无论基线血红蛋白水平如何,鲁索替尼对 MF 患者都有益处,并且该研究表明,可以考虑替代给药策略,以避免延迟对有症状的贫血 MF 患者进行鲁索替尼治疗。从治疗[立即开始受益]。本研究无法解决的一个重要临床问题是,这种剂量滴定策略是否减少了先前随机临床试验中观察到的严重血小板减少症和治疗中出现的贫血 。不幸的是,由于本试验是非随机化的,并且仅包括基线时的贫血患者,上述研究的结果不具有直接可比性,因为一组完全贫血的患者可能比人群发生血细胞减少症的风险更高COMFORT 研究的一部分,其中还包括非贫血患者。
还值得注意的是,需要增加鲁索替尼剂量的患者往往比没有增加剂量的患者具有更大的脾脏。因此,在需要 JAK 抑制剂治疗的贫血 MF 患者中,鲁索替尼初始剂量的选择(即,标准剂量,由血小板计数决定,或在 12 周时逐步递增的较低剂量,如果需要)可以基于需要达到快速减脾的程度。因此,如果出现中度至显着但不严重的脾肿大,可以考虑采用两步给药策略的可能性。最后,对于有全身症状但无明显脾肿大的贫血患者,选择较低的鲁索替尼起始剂量(即 10 mg 每天两次)是合理可行的策略。
总之,REALIZE 研究的结果表明,鲁索替尼在贫血 MF 患者中的替代给药方案是有效且耐受良好的,强化了以下观点,即对于有脾肿大和/或全身症状的 MF 患者,没有必要推迟或因共存或治疗中出现的贫血而停止使用鲁索替尼治疗。
鲁索替尼Jakavi(Jakafi/芦可替尼)哪里有卖?如何购买正版鲁索替尼Jakavi(Jakafi/芦可替尼)?
香港致泰药业代理供应鲁索替尼Jakavi(Jakafi/芦可替尼)。香港致泰药业是经香港政府卫生署注册的药品批发商,超过30年香港药房运营经验,与全球各大制药厂建立起良好的合作关系,专注于全球新特药品进出口业务,鲁索替尼Jakavi(Jakafi/芦可替尼)价格欢迎与致泰药业联络查询。


