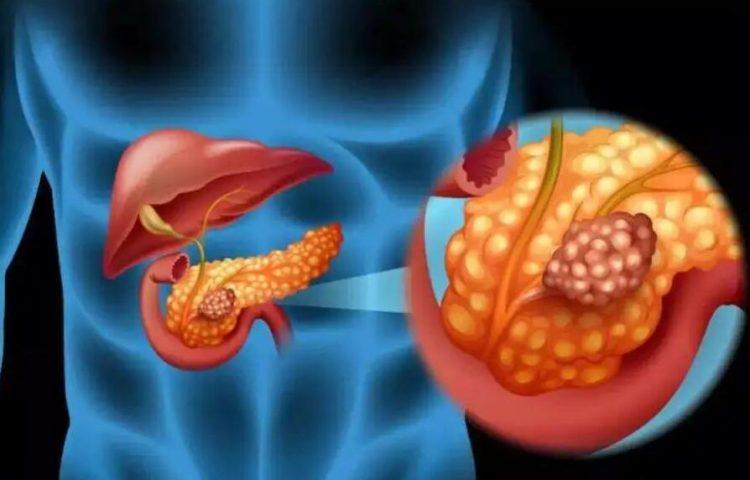
深入了解胰腺癌和恶病质
胰腺癌被认为是最致命的癌症之一,其研究和临床研究仍然是当务之急。然而,在治疗胰腺癌时,除了肿瘤本身的难以治疗外,最具挑战性的症状之一是与肿瘤无关的恶病质,或者更通俗地说,是虚弱综合症。
恶病质导致明显的肌肉质量丧失,并对胰腺癌治疗的结果产生负面影响。
“这是由显著的肌肉质量丧失所特征化的,而且它并不纯粹是营养不足。有人认为,总的来说,恶病质可能导致所有患有胰腺癌的患者中,甚至高达一半的患者死亡,”Sanjay Goel博士在接受Targeted OncologyTM采访时表示。
在这次采访中,Rutgers Robert Wood Johnson Medical School的医学肿瘤学家、一期/试验性治疗主任和医学教授Sanjay Goel博士介绍了一项旨在识别胰腺癌中恶病质机制的研究,以及这个领域未来的研究方向。
1. 胰腺癌的当前治疗格局
Goel: 胰腺癌可能是最致命的癌症之一。即使在早期被诊断的患者,不幸的是最终也面临着很高的复发风险。最终,大多数患者最终发展为晚期癌症,并在通常不到一年的时间内死于疾病。
在当前的治疗格局中,对于患有晚期胰腺癌的患者,主要是采用化疗联合疗法,有两种常用方案。一种是称为FOLFIRINOX,它是5-氟尿嘧啶、奥沙利铂和伊立替康的联合使用。这通常是为那些状态较好的患者保留的。另一种常见的组合是吉西他滨和纳帕克利taxel。这适用于可能无法耐受FOLFIRINOX的患者。通常,患者在第一线接受其中一种治疗,然后在第二线接受另一种治疗。
还有另一种选择,使用脂质体伊立替康[Onivyde],但一般来说,这不被认为非常有效。对于那些患有BRCA基因突变的罕见患者,有一种名为奥拉帕尼[ Lynparza]的药物可以使用。如果患者在经历了这些疗法后仍然身体状况良好,还可以选择参与临床试验。
2. 为什么胰腺癌治疗如此困难?
Goel: 迄今为止,我们尚未发现或发现任何此癌症中被认为是可药物干预的突变,与非小细胞肺癌或甚至更接近胰腺的另一种[胃肠相关]癌症,即胃癌不同。除了BRCA,目前没有其他可药物干预的突变。我认为胰腺癌的另一个主要问题是,大多数情况下,当它被发现,或者患者出现症状并向医疗系统寻求帮助时,[癌症]已经进展到晚期。这使得治疗变得极为具有挑战性。
另一个重要问题是胰腺癌周围存在大量的纤维化,肿瘤微环境对免疫细胞的浸润并不友好。因此,尽管经过多年的努力,免疫疗法在改善其他癌症类型的预后方面发挥了相当重要的作用,但在治疗胰腺癌方面却是一个重大挑战。
绝大多数[患有]胰腺癌的患者实际上最终会出现一种称为恶病质的临床病症,这是一种主动的、分解的过程,简单地说,就是身体开始自我分解。这表现为明显的肌肉质量丧失,而且它并不纯粹是营养不足。有人认为,总的来说,恶病质可能导致所有患有胰腺癌的患者中,甚至高达一半的患者死亡。
3. 该研究的目标是什么?
Goel: Caris [Life Sciences]是一家生物诊断公司,拥有一流的下一代测序平台。直到现在,大多数都是在肿瘤组织上进行的。几年前,他们推出了所谓的精准肿瘤学联盟[POA],与学术医生合作,真正尝试利用他们拥有的庞大组织样本来回答一些关键的临床问题。这被分为几个不同的组,我很幸运能成为胃肠组的一部分。
Caris POA在[2024 ASCO胃肠癌研讨会(ASCO GI)]上进行了几次报告。这个特定摘要的一个想法是在更详细地研究患有胰腺癌的患者的恶病质,并利用从研究其他病症中失去肌肉质量的知识中获得的一些知识。例如,myostatin/activin通路已经在神经系统疾病的患者中进行了广泛研究,包括运动神经元病患者等。该项目由南加利福尼亚大学的研究人员领导,他们决定查看是否可以进行一项深入研究,研究胰腺癌患者的myostatin通路。这是主要的想法。
4. 调查结果的总结
Goel: 这种方法的新颖之处在于有一个大型数据库。由于已经对数千患者样本进行了分析,所以基本上只需要进行数据挖掘,Caris有大约9600个带有胰腺导管腺癌的样本,它们都经过了整个转录组测序和下一代DNA测序,这对所有样本来说是相当标准的。然后,根据先前的研究,有一些已知的被认为是myostatin/activin通路激活剂的基因和某些约束抑制剂的基因。专注于这些特定基因,他们得出了所谓的恶病质基因分数。他们观察了激活剂在一侧,抑制剂在另一侧,然后将患者分为4个四分位数。Caris还与保险公司和其他数据来源签订了合同,以获得整体结果。这基本上是通过保险索赔得知这些患者的整体生存状况。
然后,我们观察了一些免疫标志物,包括PD-L1,这是某些免疫疗法药物的生物标志物,突变负担,微卫星状态。在最高和最低四分位数之间发现了一些差异。但在实际应用中,很难说,因为免疫疗法在胰腺癌中尚未得到批准,除了在极少数[微卫星不稳定性高]的患者中。在恶病质分数上,与肿瘤环境中发现的炎症的程度存在关联。这种知识实际上可能用于未来的治疗。同样,他们还研究了一种称为与免疫相关的基因表达的东西。在恶病质基因分数最高的四分位数中,发现其中几种基因的表达较高。因此,这在未来可能会证明是有用的。
就生存而言,如果我们观察两种特定的蛋白质,称为SMAD3和SMAD7,它们都是SMAD家族的一部分。SMAD3被认为是恶病质途径的激活剂。正如预期的那样,发现那些SMAD3得分最高的患者实际上生存较低。另一方面,SMAD7被认为是恶病质的抑制剂,而那些SMAD7得分最高的患者生存较好。这将是主要的发现。除此之外,他们还研究了恶病质分数与脂代谢基因之间的相关性。
总的来说,我可以说,从这些试验中最终找到的是SMAD3和SMAD7的表达,这与恶病质有关,对生存产生影响。另一件事是恶病质基因与脂代谢基因和炎症标志物之间存在联系。然而,在临床翻译方面,至少在一个方面上,我会说结果有点令人失望。曾经有一项试验研究来自Eli Lilly and Company和Loxo Oncology, Inc.的一种可以抑制myostatin的药物。有趣的是,即使在神经系统疾病患者中的临床试验中,它似乎有积极的结果;当它在患有胰腺癌的患者中进行研究时,发现在生存方面没有差异。至少在那种特定药物中,这种方法并不成功。但我认为这些数据可以进一步带领我们,并可能考虑使用SMAD3的抑制剂或SMAD7的激活剂来尝试对抗恶病质的不同途径。
另一种方法可能是进一步挖掘数据,看看恶病质与炎症之间的关系,或者恶病质与脂代谢途径之间的关系,然后从那里深入研究,看看是否有哪些可以使用的。有趣的是,20多年前就有人提出,如果我们能找到一种阻止或阻断恶病质的方法,那可能比开发所谓的化疗联合疗法更好。
在对胰腺癌和恶病质的深入研究中,我们看到了一系列的困难和挑战。胰腺癌作为一种高度致命的癌症,其治疗局面异常复杂。缺乏可靶点的突变和肿瘤微环境的不友好使得治疗变得艰难。而其中最棘手的问题之一便是恶病质,这种症状与肿瘤本身无关,却对治疗产生了深远的影响。
当前治疗中,化疗联合疗法仍然是胰腺癌的主要手段,但其局限性和效果有限。胰腺癌缺乏被认为是可药物干预的突变,与其他癌症相比更加难以治疗。此外,大多数情况下,患者在发现症状并就医时,癌症已经发展到晚期,使得治疗变得更加困难。
研究者们通过Caris Life Sciences的平台进行了一项有趣的研究,旨在深入了解胰腺癌患者的恶病质机制。通过分析大量患者样本,研究团队从中挖掘了恶病质相关的基因表达,得到了称为恶病质基因分数的指标。这项研究的目标是寻找可能影响患者生存和治疗反应的生物标志物。
研究结果表明,SMAD3和SMAD7这两种与恶病质相关的蛋白质对患者的生存状况产生了影响。具体而言,SMAD3被认为是恶病质通路的激活剂,而高得分的患者生存较低。相反,SMAD7则是恶病质的抑制剂,高得分的患者生存较好。这一发现为未来的治疗提供了新的方向,可能会考虑使用SMAD3的抑制剂或SMAD7的激活剂来干预恶病质过程。
尽管某些药物试图通过抑制myostatin来干预恶病质,但研究者发现在某些药物中,这种策略并不成功。然而,通过深入挖掘恶病质与炎症、脂代谢途径之间的关系,或许可以找到新的治疗靶点。这些研究不仅有助于理解胰腺癌和恶病质的复杂性,也为未来的个体化治疗提供了有益的线索。
综合而言,胰腺癌和恶病质的研究仍然是一个充满挑战但又备受关注的领域。通过不断深入的科学研究,我们或许能够揭开这些疾病的奥秘,为患者提供更有效的治疗方案。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请谘询主治医师。