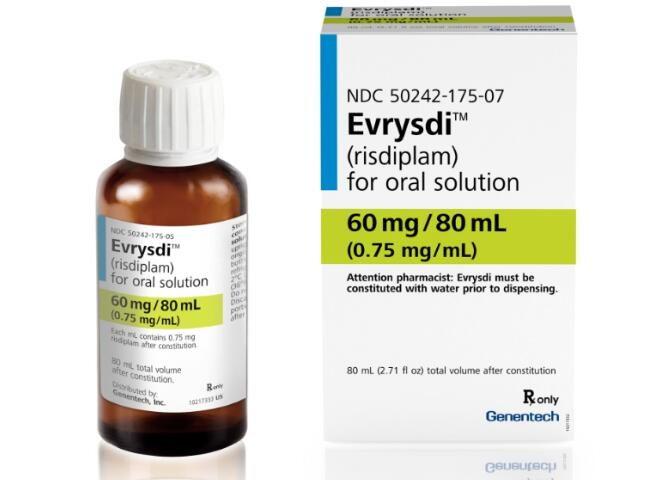
欧洲药品管理局建议将基因泰克的Evrysdi用于所有年龄段的脊髓性肌萎缩症患者
脊髓性肌萎缩症(SMA)是一种严重的进行性神经肌肉疾病,影响着婴儿和儿童的生活质量。近日,欧洲药品管理局(EMA)的人用药品委员会(CHMP)发表了一份积极的意见,建议扩大基因泰克公司的Evrysdi(risdiplam)的适应症,将其用于两个月以下的新生儿和婴儿,他们患有遗传证实的脊髓性肌萎缩症或带有一到四个拷贝的生存运动神经元(SMN)2基因。
目录
Evrysdi治疗SMA的积极效果
CHMP在审查了RAINBOWFISH试验的中期数据后,对Evrysdi的扩大适应症提出了积极的建议。据该试验显示,大多数症状前的婴儿在接受治疗后一年内可以站立或行走,这与健康婴儿进行此类活动的典型时间范围相符。对于患有SMA的婴儿而言,早期治疗对于帮助他们进行日常活动如坐、站和走等,具有极大的意义。
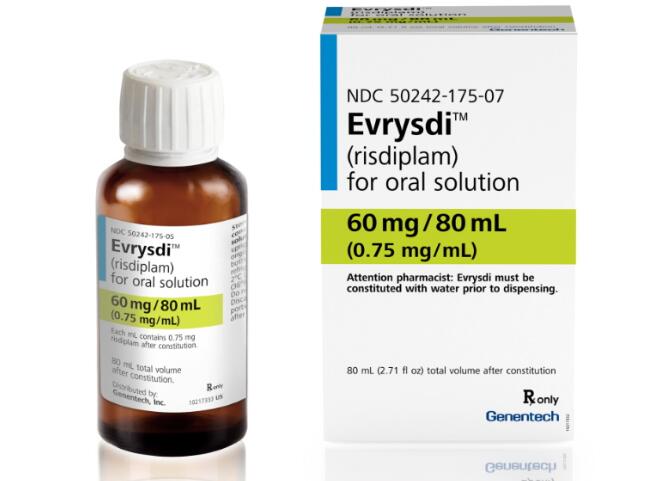
以上图片来源于网络
Evrysdi的作用机制与疾病背景
脊髓性肌萎缩症是由SMN1基因突变引起的,发病年龄及严重程度可能取决于患儿身体的SMN2基因拷贝数。这些基因的异常导致SMN蛋白缺乏,而这对于运动神经元的正常功能至关重要。Evrysdi是一种SMN2剪接修饰剂,旨在治疗由这些遗传异常引起的脊髓性肌萎缩症。该药物已经在欧盟获得批准,用于至少两个月大的SMA患者。
CHMP建议的意义与展望
如果欧盟委员会根据CHMP的建议批准Evrysdi的扩大适应症,这将是对新生儿和婴儿SMA患者的一大福音。他们将从出生开始就有机会接受这种治疗,有望改善其生活质量并提高日常活动能力。Evrysdi的积极效果将为患有SMA的患者带来新的希望,而这对于每年受到影响的数千名儿童和家庭来说,将是一个重大的突破。
脊髓性肌萎缩症是一种令人担忧的疾病,但基因泰克公司的Evrysdi给予我们对未来治疗的希望。CHMP的积极建议为这项治疗的扩大适应症铺平了道路,将使更多的患者能够受益于这一疗法。随着药物研究和医疗技术的不断进步,相信未来在SMA治疗领域将会有更多的突破和进展。我们期待着欧盟委员会在今年晚些时候做出决定,希望Evrysdi能够为SMA患者带来更美好的未来。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请谘询主治医师。