LITFULO RITLECITINIB
【商品名称】:LITFULO
【通用名称】:RITLECITINIB
LITFULO-RITLECITINIB说明书
【Litfulo(ritlecitinib)生产厂家】
辉瑞公司
【Litfulo(ritlecitinib)适应症】
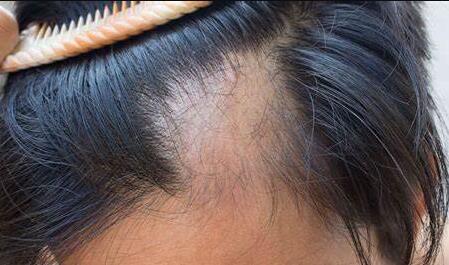
Litfulo是一种激酶抑制剂,用于治疗成人和12岁及以上青少年的严重斑秃。
使用限制:
不推荐与其他JAK抑制剂、生物免疫调节剂、环孢素或其他强效免疫抑制剂联合使用。
【Litfulo(ritlecitinib)规格】
2.5mg、5mg、10mg和15mg
【Litfulo(ritlecitinib)用法用量】
一、治疗开始前推荐的评估和免疫接种
在启动Litfulo之前进行以下评估:
①结核病(TB)感染评估:活动性TB患者不建议开始使用Litfulo。对于潜伏结核病患者或潜伏结核检测呈阴性、结核高危患者,应在开始执行 Litfulo 之前开始潜伏结核的预防性治疗。
②根据临床指南进行病毒性肝炎筛查:乙肝或丙肝患者不建议开始使用 Litfulo。
③绝对淋巴细胞计数(ALC)<500/mm 3 或血小板计数<100,000/mm 3时不应使用Litfulo。
④根据当前的免疫接种指南更新免疫接种。
二、推荐剂量
Litfulo的推荐剂量:每日一次口服50mg,伴或不伴食物。整个吞下胶囊。请勿压碎、打开或咀嚼Litfulo胶囊。如果漏服一次,应尽快补服,除非距下一次给药不到8小时,在这种情况下,跳过漏服的剂量。此后,在正常的预定时间恢复给药。
三、用药过量
在临床试验中,Litfulo的单次口服剂量高达800毫克。不良反应与在较低剂量下观察到的不良反应相当,未发现特定毒性。健康成年志愿者单次口服800 mg(含)的药代动力学(PK)数据表明,超过90%的给药剂量有望在48小时内消除。Litfulo过量没有特效解毒剂。治疗应该是对症和支持性的,并监测患者不良反应的体征和症状。
四、 严重肝损害患者
Litfulo不推荐用于重症患者(Child Pugh C)肝损害。
五、 治疗中断或终止
如果需要中断治疗,预计短于6周的暂时治疗中断不会导致再生头皮毛发的显著减少。建议在治疗开始前和治疗开始后4周进行ALC和血小板计数,之后根据常规患者管理进行。
血液学异常:关于因血液学异常而中断或停用Litfulo治疗的建议总结于表1。
表1、实验室监测指南

【Litfulo(ritlecitinib)禁忌症】
已知对Litfulo或其任何赋形剂过敏的患者禁用Litfulo。
【Litfulo(ritlecitinib)作用机制】
Litfulo是一种激酶抑制剂。
Ritlecitinib通过阻断三磷酸腺苷(ATP)结合位点,不可逆地抑制Janus激酶3 (JAK3)和肝细胞癌(TEC)激酶家族中表达的酪氨酸激酶。在细胞环境中,ritlecitinib抑制由JAK3依赖性受体介导的细胞因子诱导的STAT磷酸化。此外,ritlecitinib抑制依赖于TEC激酶家族成员的免疫受体的信号传导。目前尚不清楚抑制特定JAK或TEC家族酶与治疗效果的相关性。
【Litfulo(ritlecitinib)贮藏】
将Litfulo储存在20℃至25℃的温度范围内,允许在15℃至30℃的温度范围内波动。
【Litfulo(ritlecitinib)注意事项】
一、 严重感染
据报道,接受Litfulo治疗的患者出现了严重感染。最常见的严重感染是阑尾炎、新冠肺炎感染(包括肺炎)和败血症。在机会性感染中,Litfulo报告了多发性皮肤带状疱疹。患有活动性严重感染的患者应避免使用Litfulo。在对以下患者开始使用Litfulo之前,请考虑治疗的风险和益处:慢性或复发性感染患者;接触过结核病患者;有严重感染或机会性感染史患者;曾在结核病或真菌病流行地区居住或旅行过,或患有可能导致感染的潜在疾病患者。
在使用Litfulo治疗期间和之后密切监测患者的感染体征和症状的发展。如果患者出现严重或机会性感染,请中断Litfulo。在使用Litfulo治疗期间出现新感染的患者应接受适合于免疫功能低下患者的及时和完整的诊断检测,应开始适当的抗菌治疗,并应密切监测患者。一旦感染得到控制,Litfulo可能会恢复。
在开始治疗之前,对患者进行结核病筛查。Litfulo不应用于活动性肺结核患者。对于新诊断为潜伏性结核或之前未经治疗的潜伏性结核患者,应在开始使用Litfulo治疗之前开始抗结核治疗。对于潜伏结核试验阴性的患者,在开始对高危患者使用Litfulo治疗前考虑抗结核治疗,并考虑在使用Litfulo治疗期间筛查结核高危患者。
病毒再激活:在临床试验中报告了病毒再激活,包括疱疹病毒再激活的病例(如带状疱疹)]。如果患者出现带状疱疹,考虑中断治疗,直到症状缓解。
在开始使用Litfulo治疗之前,应根据临床指南进行病毒性肝炎筛查。有HIV感染或乙肝或丙肝感染证据的患者被排除在临床试验之外。
二、 死亡率
在一项针对50岁及以上至少有一种心血管危险因素的RA患者的另一种JAK抑制剂的大型随机上市后安全性研究中,观察到接受JAK抑制剂治疗的患者比接受TNF阻滞剂治疗的患者的全因死亡率(包括心血管猝死)更高。在开始或继续使用Litfulo治疗前,考虑患者个体的益处和风险。
三、 恶性肿瘤和淋巴增生性疾病
在Litfulo的临床试验中观察到恶性肿瘤,包括非黑色素瘤皮肤癌(NMSC)。在一项针对RA患者的另一种JAK抑制剂的大型随机上市后安全性研究中,观察到接受JAK抑制剂治疗的患者与接受TNF阻滞剂治疗的患者相比,恶性肿瘤(不包括非黑色素瘤皮肤癌(NMSC))的发生率更高。与用TNF阻滞剂治疗的患者相比,用JAK抑制剂治疗的患者中观察到较高的淋巴瘤发生率。与用TNF阻滞剂治疗的那些人相比,在用JAK抑制剂治疗的现在或过去的吸烟者中观察到更高的肺癌发生率。在这项研究中,目前或过去吸烟者患恶性肿瘤的风险增加。在对除成功治疗的NMSC或宫颈癌以外的已知恶性肿瘤患者开始或继续治疗前,应考虑利替尼治疗的风险和益处。对于皮肤癌风险增加的患者,建议进行定期皮肤检查。
四、 主要心血管不良事件(MACE)
在另一项针对至少有一项心血管危险因素的50岁及以上RA患者的JAK抑制剂的大型随机上市后安全性研究中,观察到JAK抑制剂治疗的主要心血管不良事件(MACE)发生率(定义为心血管死亡、非致死性心肌梗死(MI)和非致死性中风)高于TNF阻滞剂治疗的患者。目前或过去吸烟的患者面临额外的风险增加。在开始或继续使用Litfulo治疗之前,请考虑患者个体的益处和风险,尤其是目前或过去吸烟的患者以及具有其他心血管风险因素的患者。应告知患者严重心血管事件的症状以及发生时应采取的措施。患有心肌梗死或中风的患者应停止使用Litfulo。
五、 血栓栓塞事件
在接受Litfulo的患者中报告了一例肺栓塞(PE)事件。Litfulo高剂量组,有1例报告视网膜动脉阻塞事件。在一项大规模、随机、上市后安全性研究中,另一种JAK抑制剂在50岁及以上至少有一个心血管危险因素的类风湿关节炎患者中的应用,观察到与接受TNF阻滞剂治疗的患者相比,总体血栓形成、DVT和PE的发生率更高。对于可能增加血栓形成风险的患者,应避免使用Litfulo。如果出现血栓或栓塞的症状,患者应中断Litfulo,并及时进行评估和适当的治疗。
六、 超敏反应
在临床试验中,Litfulo患者观察到了严重的反应,包括过敏反应、荨麻疹和皮疹。如果发生临床上显著的过敏反应,停止使用Litfulo,并实施适当的治疗。
七、 实验室异常
Litfulo治疗与淋巴细胞和血小板的减少有关。在 Litfulo开始前,进行Alcon和血小板计数。Litfulo开始治疗后,根据Alcon和血小板计数,建议中断或停止治疗异常。
肝酶升高:与安慰剂相比,Litfulo治疗与肝酶升高的发生率增加有关。ALT升高≥5倍正常上限(ULN)和AST升高≥5次在Litfulo临床试验中观察到ULN。在基线和之后根据常规患者管理进行评估。建议立即调查肝酶升高的原因,以确定潜在的药物性肝损伤的情况。如果观察到ALT或AST升高,并怀疑药物性肝损伤,则中断Litfulo直到排除此诊断。
肌酸磷酸激酶(CPK)升高——与安慰剂相比,Litfulo治疗与CPK升高的发生率增加有关。
八、 接种疫苗
没有关于接受Litfulo治疗的患者对疫苗接种反应的数据。在开始治疗期间或治疗前不久应避免使用减毒活疫苗。在开始Litfulo之前,建议患者接受所有免疫接种,包括预防性带状疱疹疫苗接种,以符合当前的免疫指南。
【Litfulo(ritlecitinib)不良反应】
1、Litfulo的副作用包括:头痛、腹泻、痤疮、皮疹、荨麻疹、“毛发突起”(毛囊炎)、发热、皮肤瘙痒和炎症(特应性皮炎)、头晕、血液肌酸磷酸激酶增加、带状疱疹、红细胞计数减少以及口腔内肿胀和溃疡。
2、如有以下严重副作用,应立即就医:严重眼部症状,如突然失明、视力模糊、视野狭窄、眼睛疼痛或肿胀,或看到灯光周围有光晕;严重的心脏症状,如心跳快、不规则或剧烈;呼吸急促;以及突然头晕、头昏眼花或昏厥;严重头痛、意识模糊、口齿不清、手臂或腿部无力、行走困难、失去协调性、感觉不稳定、肌肉非常僵硬、高烧、大量出汗或颤抖。
【Litfulo(ritlecitinib)在特殊人群中使用】
1、 妊娠
在孕妇中使用Litfulo的临床试验的可用数据不足以确定重大出生缺陷、流产或其他不良母体或胎儿结果的药物相关风险。在动物生殖研究中,根据曲线下面积(AUC)比较,怀孕大鼠和兔子在器官形成期间口服ritlecitinib分别导致49倍和55倍最大推荐人类剂量(MRHD)的胎儿毒性和胎儿畸形。
2、 哺乳期
没有关于母乳中存在ritlecitinib、对母乳喂养婴儿的影响或对泌乳量的影响的数据。Ritlecitinib存在于哺乳期大鼠的乳汁中。当一种药物存在于动物乳汁中时,它也可能存在于人乳中。由于在成人中的严重不良反应,包括严重感染和恶性肿瘤的风险,建议女性在使用Litfulo治疗期间以及最后一次给药后约14小时内(约6个消除半衰期)不要进行母乳喂养。
3、 儿科用药
Litfulo治疗12岁及以上儿童斑秃的安全性和有效性已得到证实。共有181名12岁至< 18岁的儿童患者参加了斑秃临床试验,其中105名12岁至< 18岁的儿童斑秃患者在一项关键的双盲安慰剂对照试验(AA-I试验)中随机分组。儿童患者和成人的疗效一致。儿童患者的不良反应与成人相似。尚未确定Litfulo对12岁以下儿童患者的安全性和有效性。
4、 老年用药
年龄≥65岁的患者无需调整剂量。参加斑秃试验的总共28名患者年龄在65岁及以上,没有一名患者年龄在75岁及以上。Litfulo的临床试验没有包括足够数量的65岁及以上的患者,以确定他们的反应是否与年轻成年患者不同。由于一般来说,老年人群的感染率较高,因此在治疗老年人时应谨慎。
3、 肝脏损伤
轻度(Child Pugh A)或中度(Child Pugh B)肝功能损害患者无需调整剂量。严重肝功能损害(Child Pugh C级)的患者不建议使用Litfulo。
以上资料只供参考,详情请咨询医生建议。更多药品信息可与我们的药剂师客服联系查询!
【温馨提示】
如需要更多Litfulo(ritlecitinib)资讯,欢迎与致泰药业联络查询。香港致泰药业是经香港政府卫生署注册的药品批发商,专注于全球新特药品进出口业务。